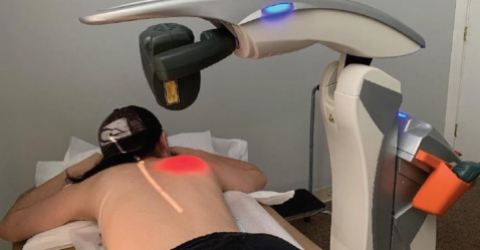
A new clinical case confirms the efficacy of MLS® for treating Covid-19 pneumonia
New studies and clinical reports confirm that MLS® Laser Therapy is useful for contributing to the treatment of patients with COVID-19 pneumonia.
Used as a complementary treatment to standard drug therapy, MLS® alleviates acute inflammatory events caused by an excessive production of pro-inflammatory cytokines and favours pulmonary functional recovery.
This is confirmed by a recent clinical case concerning a 70-year old patient admitted to hospital with symptoms of respiratory failure, cough, vomiting and chest pain, with X-ray evidence of atypical pneumonia from COVID-19. The patient underwent drug therapy combined with a daily session of MLS® Laser Therapy for 5 days and showed:
- a significant increase in the level of oxygen saturation, which went from the initial 90% to 98%;
- a general improvement of his health with a regression of symptoms;
- significant decrease of the level of ferritin, recognised as a marker of acute and chronic inflammation.
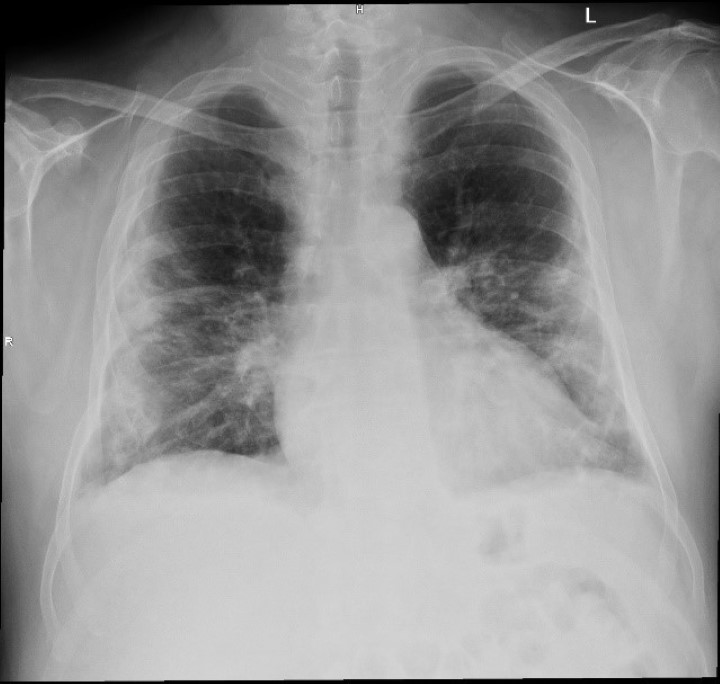
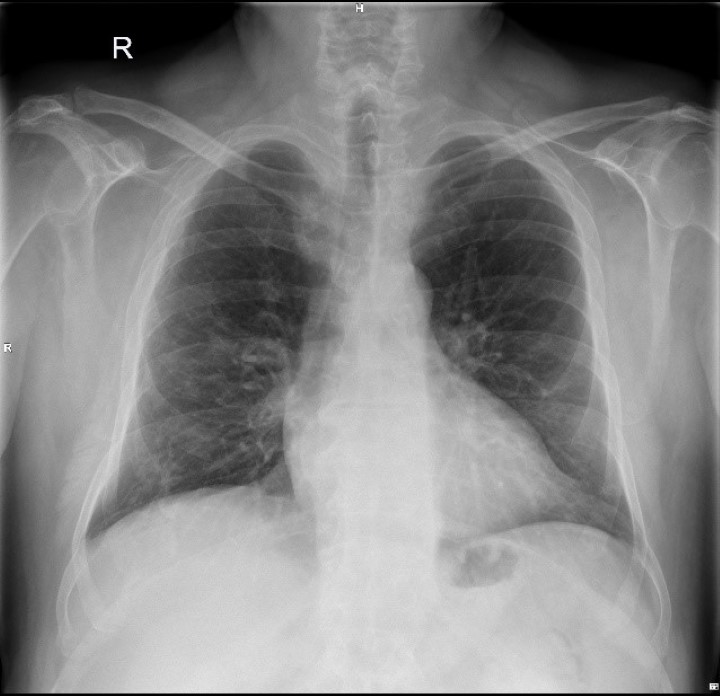
The chest X-ray carried out both before and after the laser therapy with the M6 device furthermore showed a significant reduction in inflammation (clear and extended lungs, with a decrease in consolidations and opacities). Although concerning one patient only, the results of the study support the use of MLS® Laser Therapy as an aid to manage patients with interstitial pneumonia.
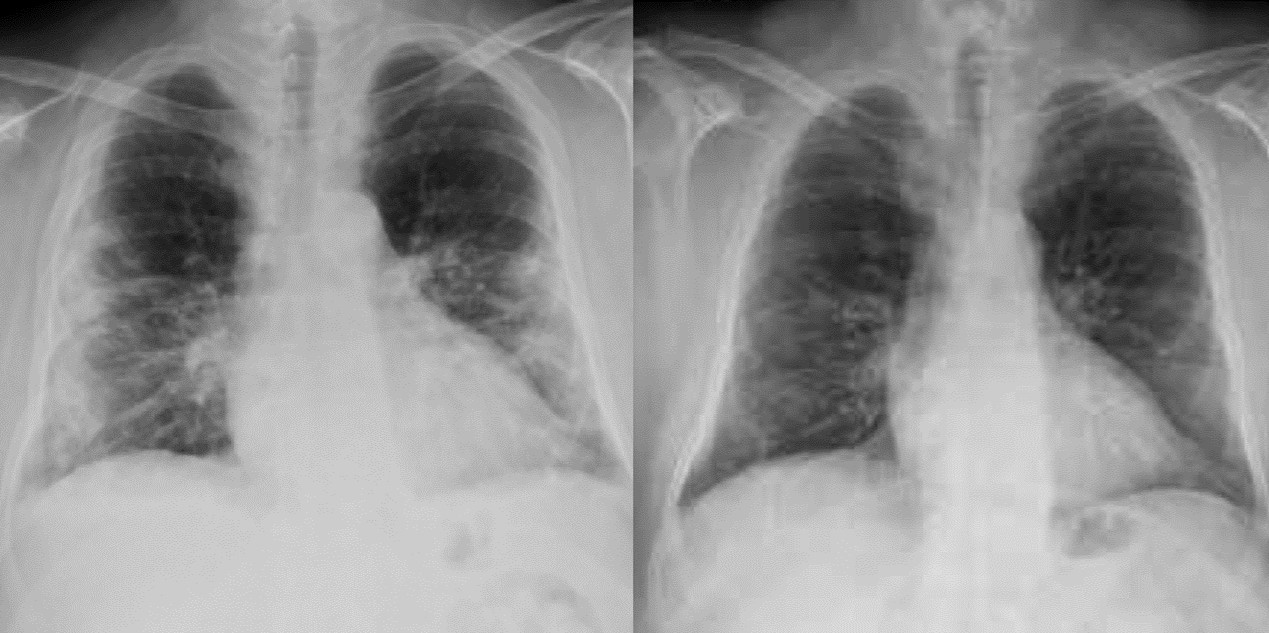
“Use of the MLS® Laser Therapy in the management of SARS-CoV-2 infection: a case report”
L. Cibulka, V. Petrtýlová
Energy For Health [21], 2021