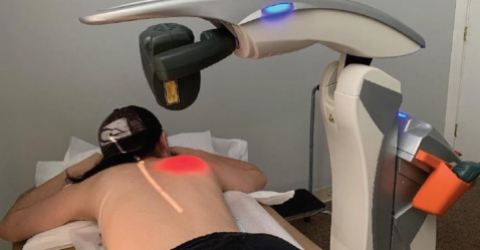
Neuer klinischer Fall bestätigt die Wirksamkeit von MLS® bei der Behandlung von Lungenentzündung durch Covid-19
12 Oktober 2021 - Forschung -
Share
Neue Studien und klinische Berichte belegen, wie nützlich die MLS®-Lasertherapie zur Behandlung von Patienten mit COVID-19-Lungenentzündung ist.
Als ergänzende Behandlung zur medikamentösen Standardtherapie lindert MLS® akute Entzündungserscheinungen, die durch die übermäßige Produktion von entzündungsfördernden Zytokinen verursacht werden, und fördert die funktionelle Erholung der Lunge.
Ein Beweis dafür ist ein kürzlich veröffentlichter klinischer Fall, bei dem ein 70-jähriger Patient mit Symptomen von Atemnot, Husten, Erbrechen und Brustschmerzen ins Krankenhaus eingeliefert. Mit Hilfe von Röntgenaufnahmen konnte eine atypische COVID-19-Lungenentzündung nachgewiesen werden. Nach einer 5-Tage-langen medikamentösen Therapie in Kombination mit einer täglichen MLS®-Lasertherapiesitzung zeigte der Patient:
- ueinen deutlichen Anstieg der Sauerstoffsättigung, die von anfänglich 90% auf 98% stieg;
- eine allgemeine Verbesserung seines Gesundheitszustands mit Rückbildung der Symptome;
- eine signifikante Abnahme der Ferritinwerte, die als Marker für akute und chronische Entzündungen anerkannt sind.
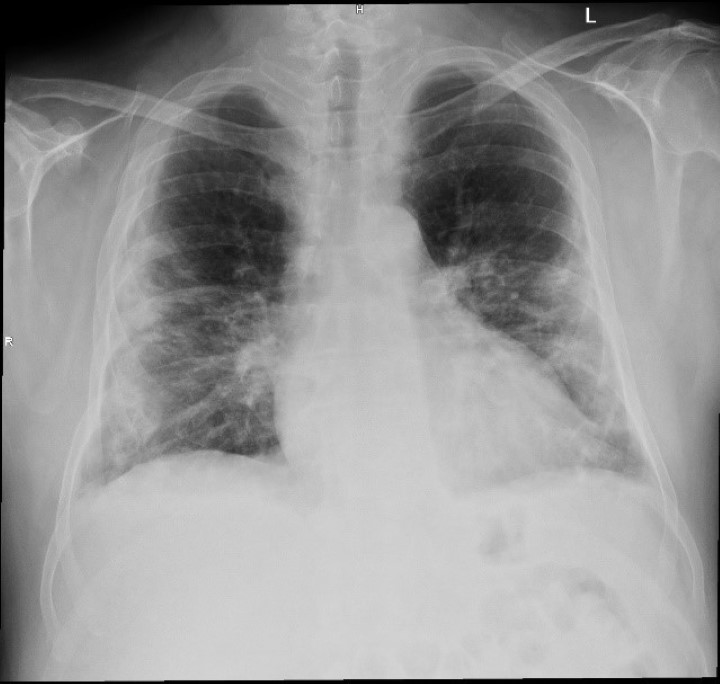
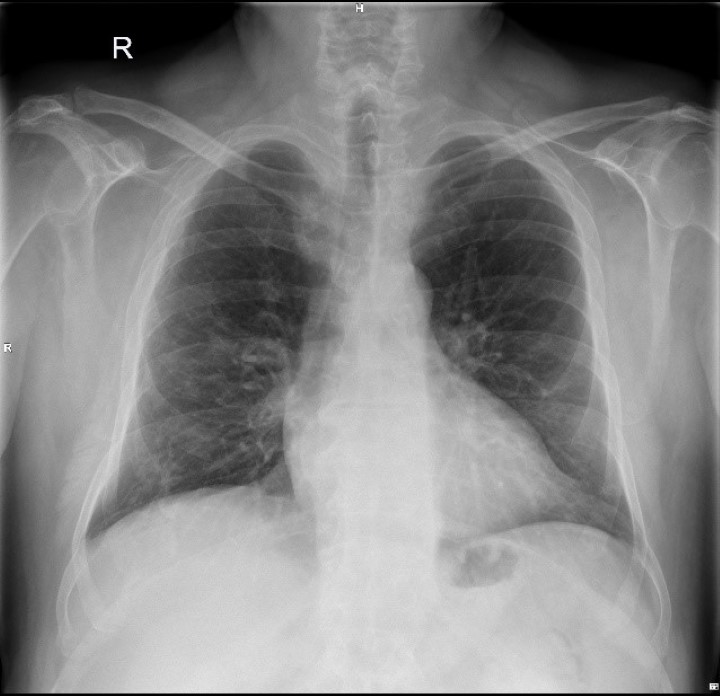
Die Kontrolle des Brustkorbs mittels Röntgenaufnahme, die vor und nach der Lasertherapie mit dem M6-Gerät durchgeführt wurde, zeigte ebenfalls eine deutliche Verringerung der Entzündung (klare, erweiterte Lungen mit verringerten Konsolidierungstrübungen). Obwohl es sich um einen einzelnen Patienten handelt, unterstützen die Ergebnisse der Studie den Einsatz der MLS®-Lasertherapie als Hilfsmittel bei der Behandlung von Patienten mit interstitiellen Pneumonien.
Testo a Destra
Immagine 30%/Testo 60%
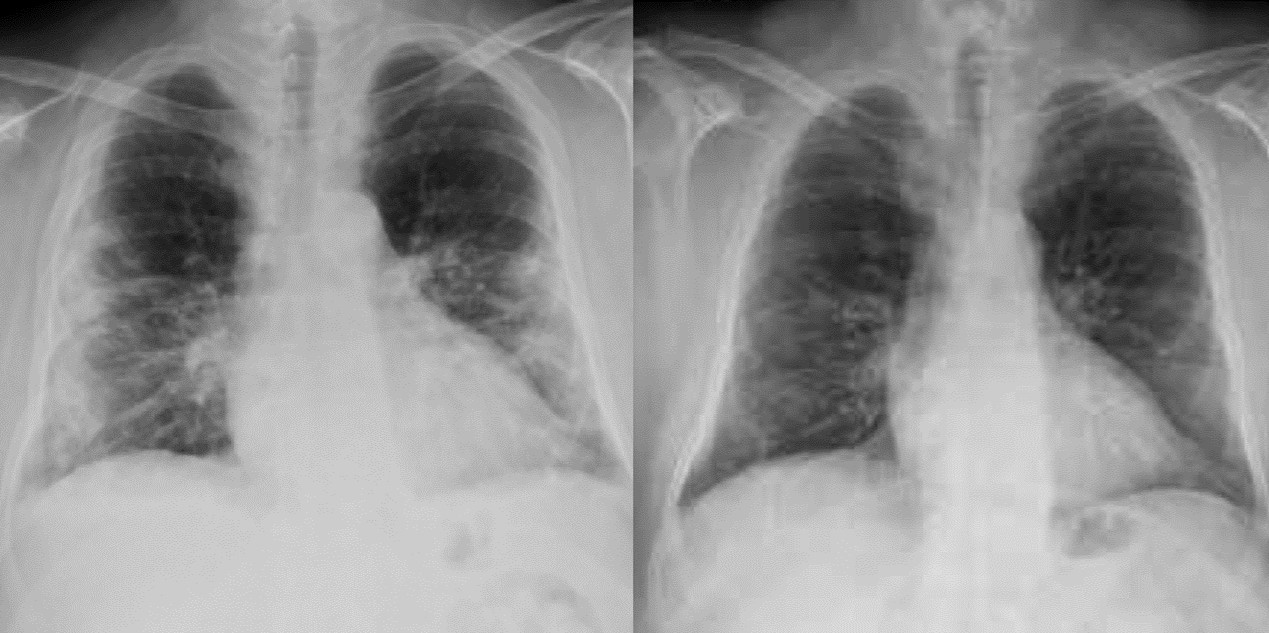
“Use of the MLS® Laser Therapy in the management of SARS-CoV-2 infection: a case report”
L. Cibulka, V. Petrtýlová
Energy For Health [21], 2021