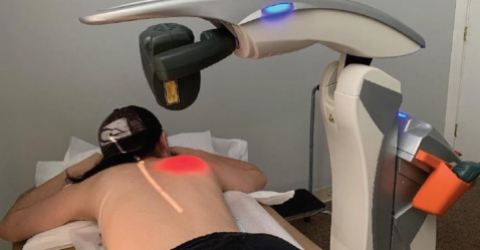
Nuevo caso clínico confirma la eficacia de MLS® en el tratamiento de la pulmonía por Covid-19
Nuevos estudios e informes clínicos demuestran que la Laserterapia MLS® es útil para ayudar a tratar a los pacientes con pulmonía por COVID-19.
Utilizado como tratamiento complementario a la terapia farmacológica estándar, MLS® tiene el efecto de aliviar las manifestaciones inflamatorias agudas causadas por la excesiva producción de citoquinas pro inflamatorias y favorece la recuperación funcional a nivel pulmonar.
Prueba de ello es el reciente informe de un paciente de 70 años ingresado en el hospital con síntomas de insuficiencia respiratoria, tos, vómito y dolor torácico y evidencia radiográfica de pulmonía atípica por COVID-19. Sometido a terapia farmacológica combinada a una sesión diaria de Laserterapia MLS® durante 5 días, el paciente mostró:
- un aumento significativo del nivel de saturación de oxígeno, pasado del inicial 90% a 98%;
- una mejoría general de su estado de salud con regresión de los síntomas;
- una disminución significativa del nivel de ferritina, reconocida como marcador de inflamación aguda y crónica.
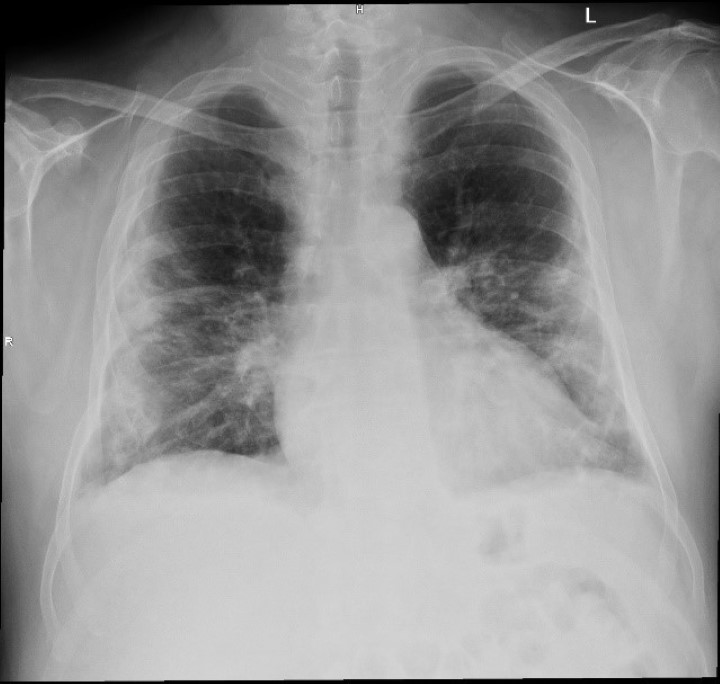
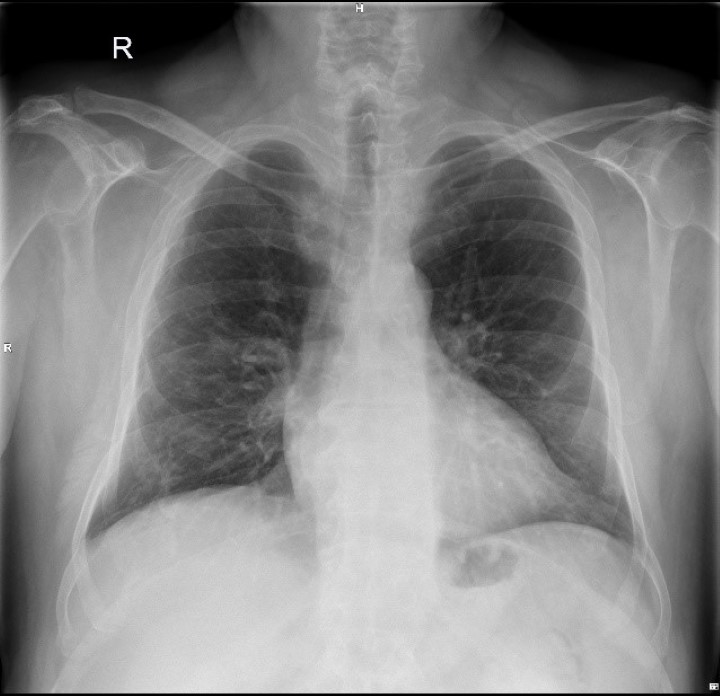
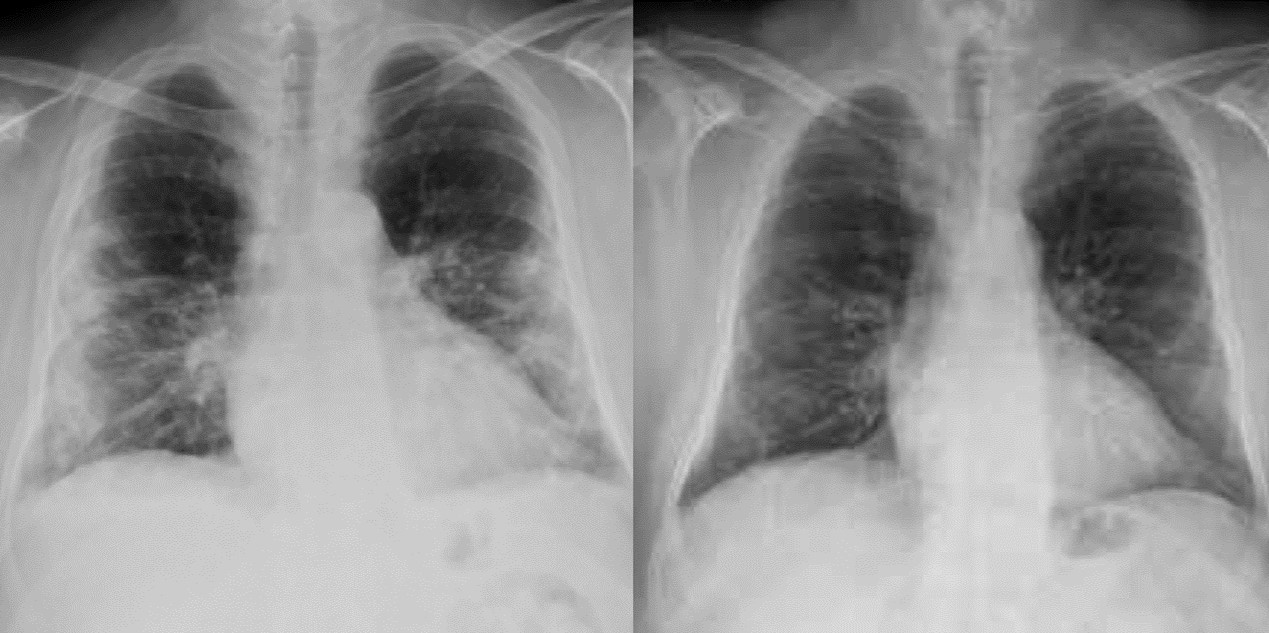
El control radiográfico del tórax, realizado antes y después de la terapia láser con el dispositivo M6, también demostró una reducción significativa de la inflamación (pulmones limpios, expandidos, con disminución de las opacidades de consolidación). Aunque solo se refiere a un paciente, los resultados del estudio apoyan el uso de la terapia láser MLS® como ayuda en el tratamiento de pacientes con pulmonía intersticial.
“Use of the MLS® Laser Therapy in the management of SARS-CoV-2 infection: a case report”
L. Cibulka, V. Petrtýlová
Energy For Health [21], 2021