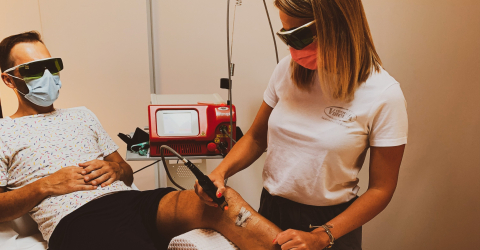
Formazione Hilterapia® in presenza per tre cliniche spagnole
05 Novembre 2021 - Formazione -
Offrire informazioni puntuali circa le caratteristiche di Hilterapia®, i suoi tangibili benefici e, contemporaneamente, dare indicazioni per il miglior impiego di HIRO 3.0 al personale di diverse cliniche spagnole del gruppo Asepeyo: con questo obiettivo lo staff ASA si è attivato per supportare il distributore locale Prim in un’attività formativa svoltasi a più riprese, inizialmente da remoto e solo recentemente in presenza.
“Per ottimizzare il percorso formativo – spiega Roberto Terruzzi, Senior Area Manager ASA – sono state inizialmente previste delle sessioni di training online durante le quali è stata data una prima introduzione teorica sulla terapia. Successivamente si è proceduto con un intervento in presenza rivolto a tutto il personale del servizio di fisioterapia delle cliniche di Madrid e Barcellona facenti parte del gruppo Asepeyo. A questi due team si è aggiunto quello della struttura di Marbella che, come le altre due, può contare su un dispositivo HIRO 3.0”.





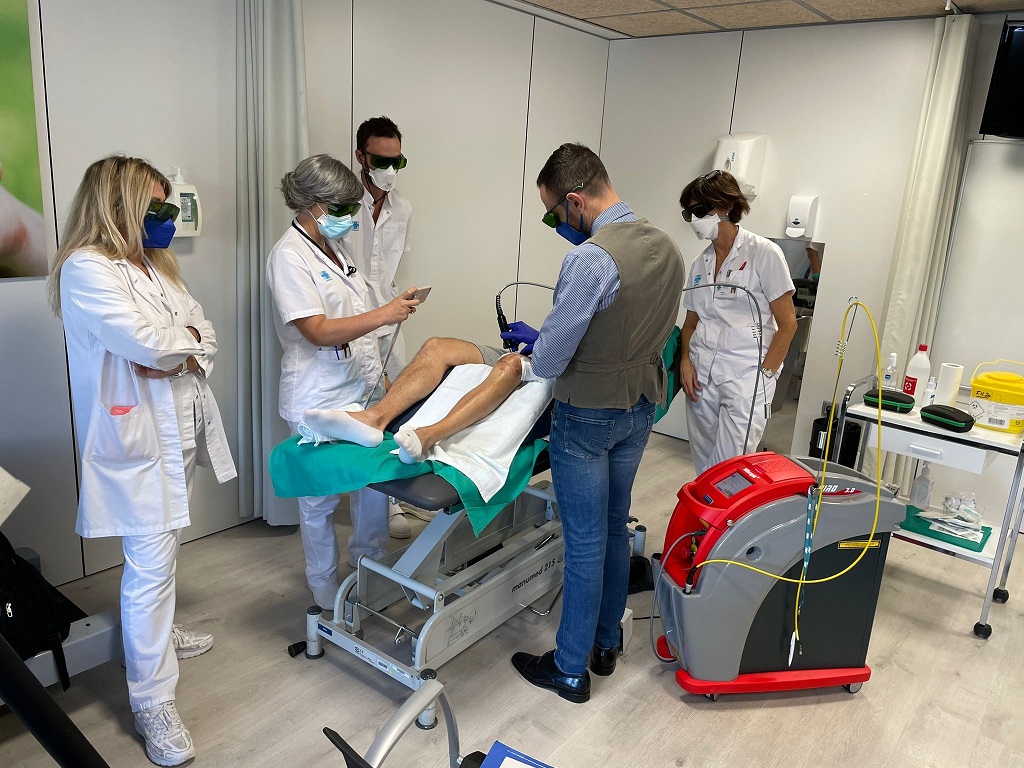
Significativi i riscontri positivi raccolti a chiusura del corso, che ha visto un’attiva partecipazione da parte di tutti i presenti.
“A confermare l’interesse dei fisioterapisti sono state le numerose domande che ci sono state rivolte, prevalentemente funzionali a migliorare l’impiego di Hilterapia® nel quotidiano nel trattare specifiche patologie e a condurre con massima efficacia le sessioni terapeutiche”.