Le dispositif MiS vainc un ulcère diabétique chronique: un cas clinique
Après avoir été testée et largement utilisée dans le traitement des plaies avec des résultats appréciables, la Thérapie Laser MLS®, par le biais du dispositif MiS, a également donné des résultats positifs dans le traitement d'un cas d'ulcère diabétique chronique.
L'action concomitante de deux longueurs d'onde différentes avec la puissance de pointe élevée caractéristique de l'appareil produit des effets analgésiques, anti-inflammatoires et anti-œdémateux, qui se sont avérés importants pour la gestion efficace de la pathologie et pour faciliter la réparation des tissus superficiels et profonds.
Ceci est illustré par le cas d'une patiente de 65 ans souffrant de diabète sucré de type II et présentant un ulcère chronique à la cheville droite causé par la maladie. D'abord soumise sans résultats appréciables à un traitement médicamenteux et à une surveillance spécialisée, la patiente a ensuite été soumise à la thérapie laser MLS®: 20 séances (4 par semaine, chacune durant 2 minutes) avec le dispositif MiS (protocole «plaie superficielle»), suivies d'un simple pansement, ont produit dès les premières séances une amélioration évidente de l'ulcère, jusqu'à sa fermeture complète en fin de cycle.
Les suivis ultérieurs, à 1 et 2 mois d'intervalle, ont également montré un rétablissement total de la barrière cutanée et l'absence d'inflammation.
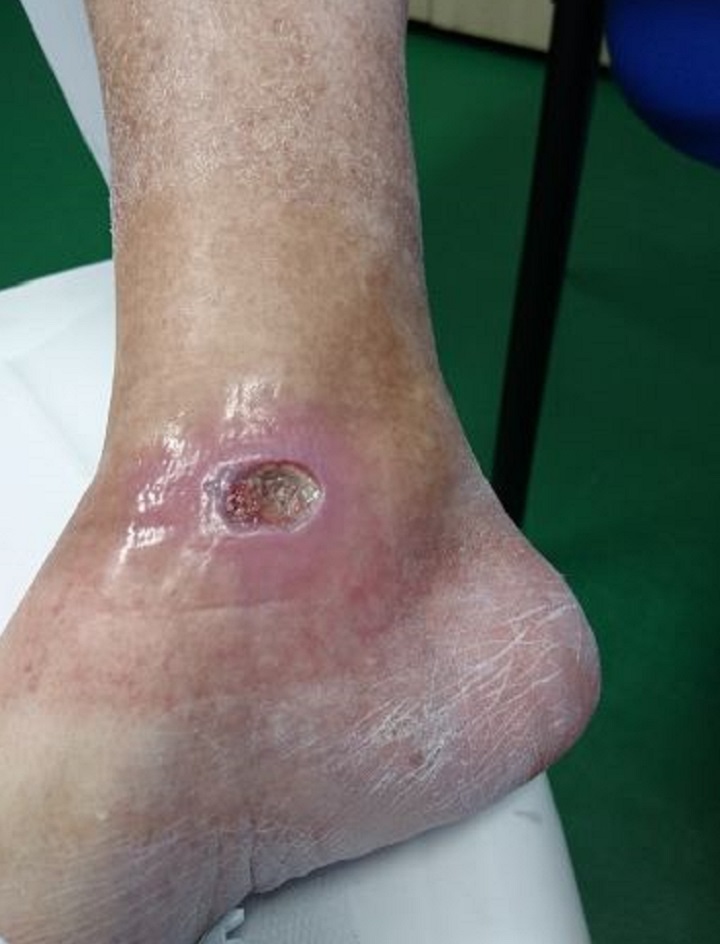
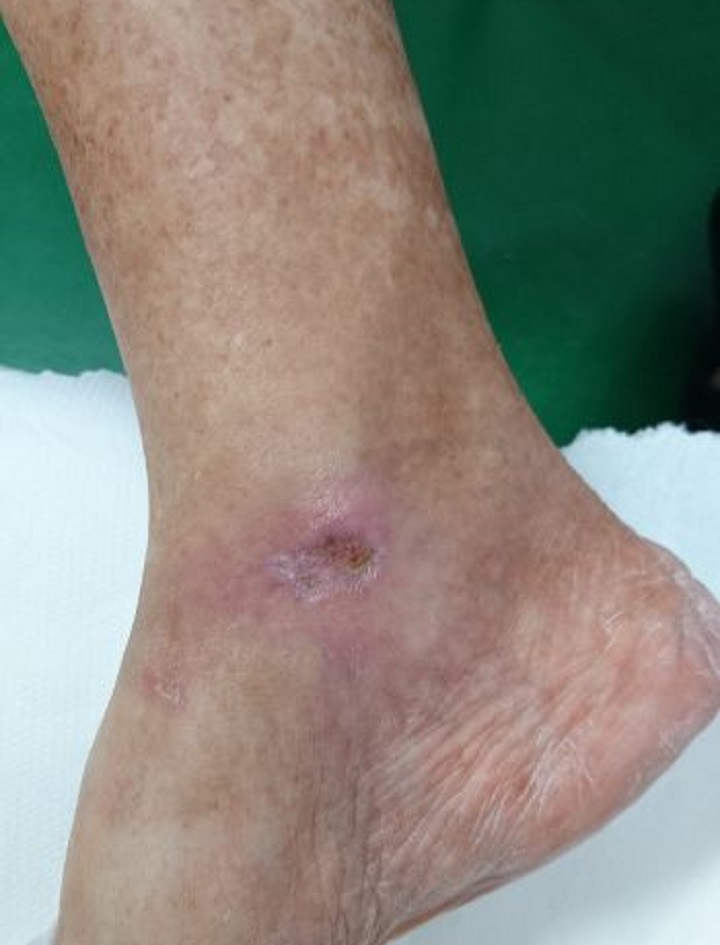
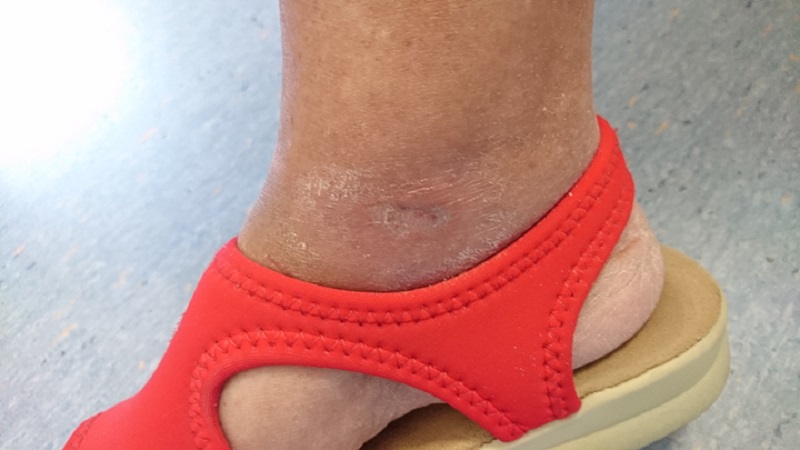
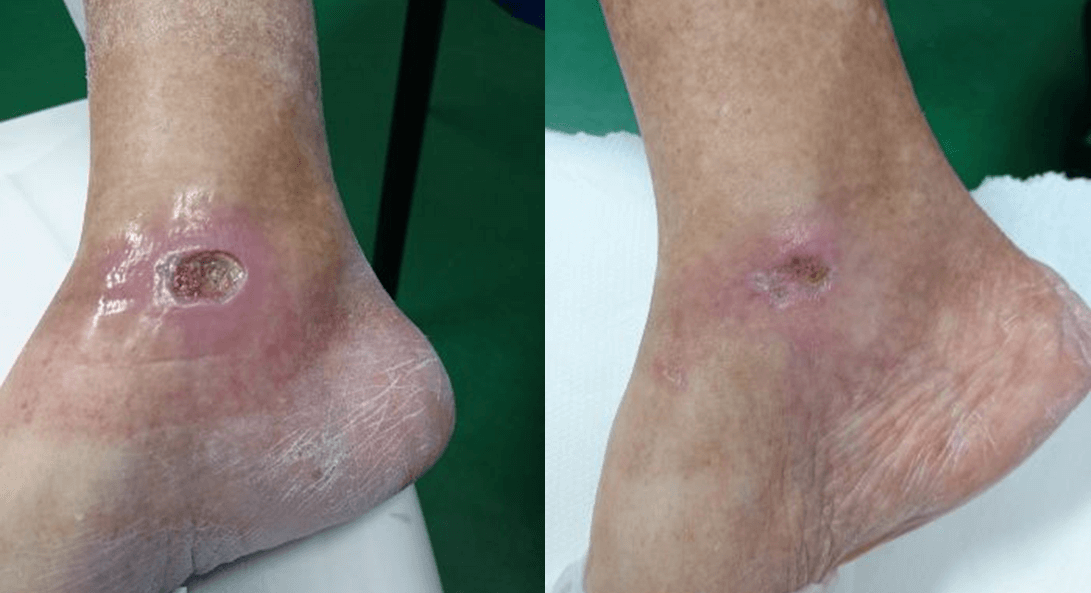
“Healing of Leg Diabetic ulcer treated with MLS-MiS laser (MiS – MLS® High Peak Pulse): a case report”
T. Viliani, B. Lombardi
Energy For Health [21], 2021