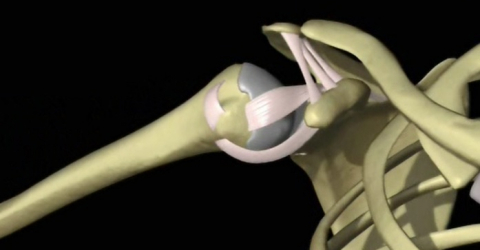
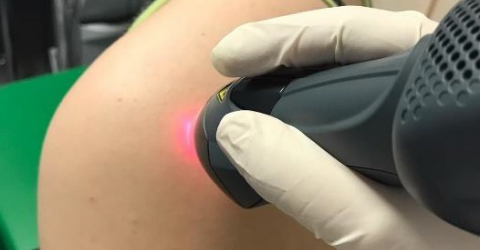
MLS® at the forefront in treating subacromial pain syndrome
A recent research - The Short-Term Outcomes of Multiwave Locked System (MLS) Laser Therapy versus a Combination of Transcutaneous Nerve Stimulation and Ultrasound Treatment for Subacromial Pain Syndrome – carried out on a significant number of patients affected by subacromial pain syndrome (SAPS) highlighted the effectiveness of MLS® for its treatment.
In fact, after the application of MLS® Laser Therapy the following was observed:
- improved functionality
- reduced pain
- reduced disability in the short term
In order to reach this result, 47 people affected by this pathology were divided into two groups each with its own therapeutic solution: the 22 patients in the first group underwent 10 5-minute sessions with MLS® to which some exercises were added, whilst the remaining 25 in the second group underwent TENS/ultrasound sessions and physical exercise.
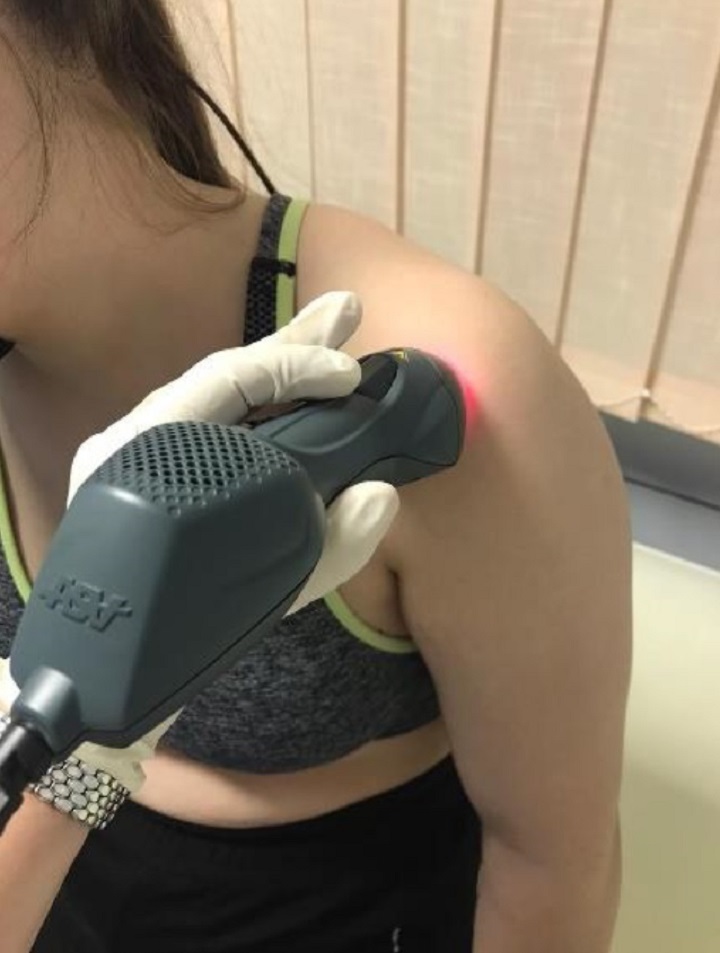
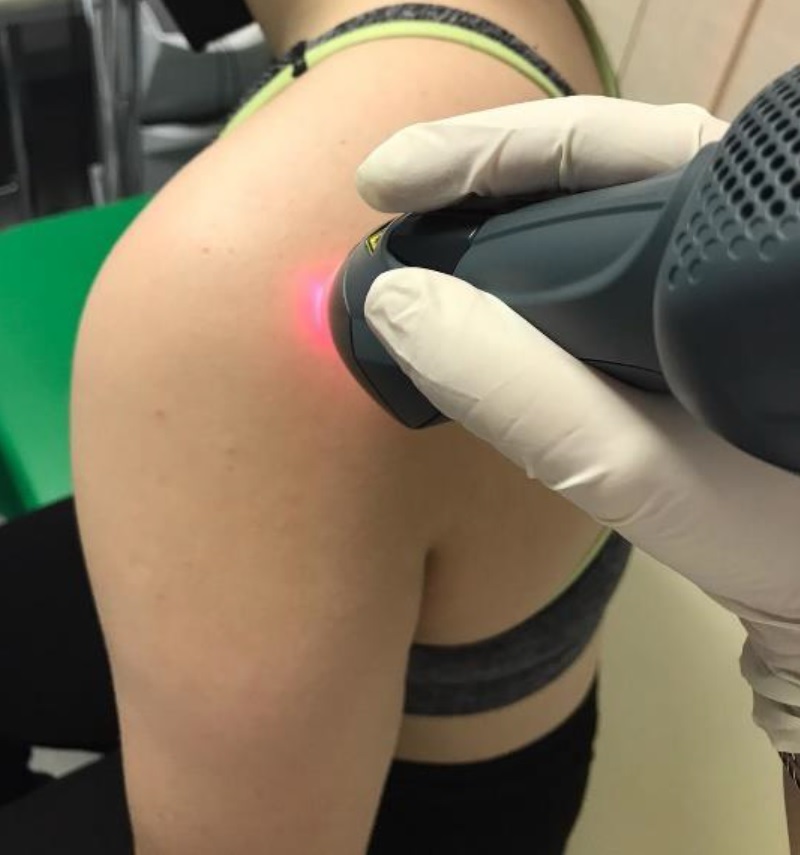
To evaluate the outcome of the two therapies, before treatment and at 15 days from the end of the cycles, the values of 3 significant parameters were assessed: VAS (pain), CSS score (functionality), SPADI score (pain and disability).
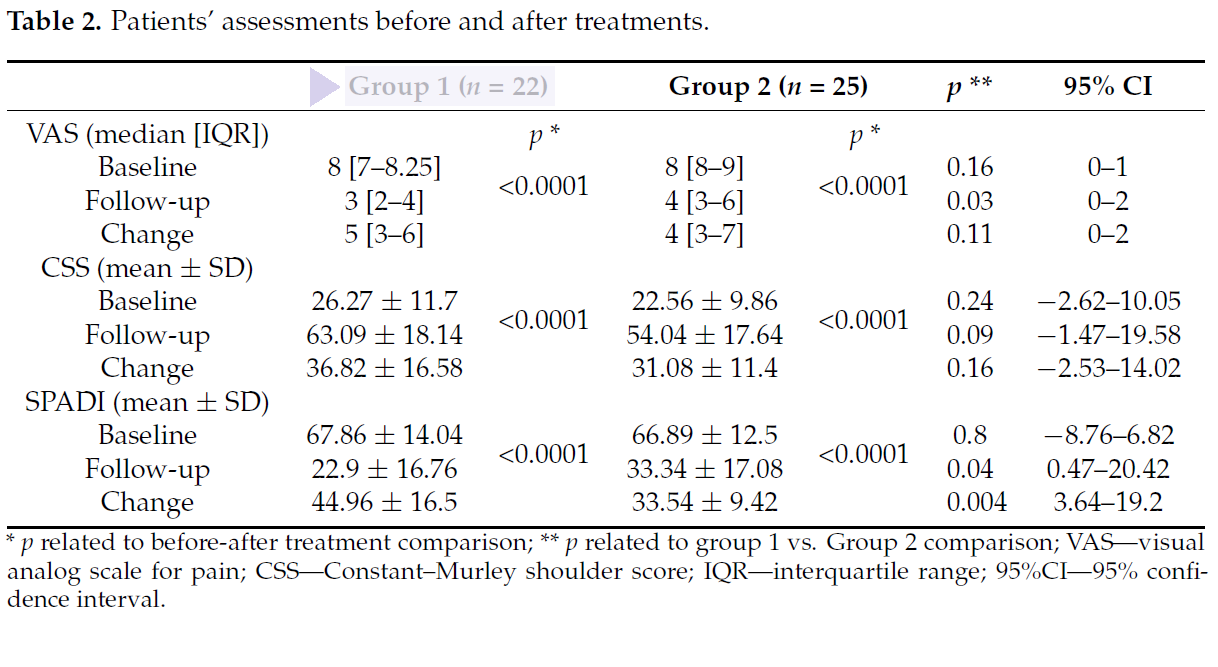
The conclusion reached was that although both treatments were suitable and valid, MLS® Laser Therapy combined with physical therapy exercises achieved significantly better scores for VAS and SPADI compared with the other combined solution (TENS/ultrasound and physical exercise).