MLS® and COVID-19: a new success in treating interstitial pneumonia
A new case confirms the effectiveness of MLS® as supporting therapy for treating pneumonia caused by COVID-19.
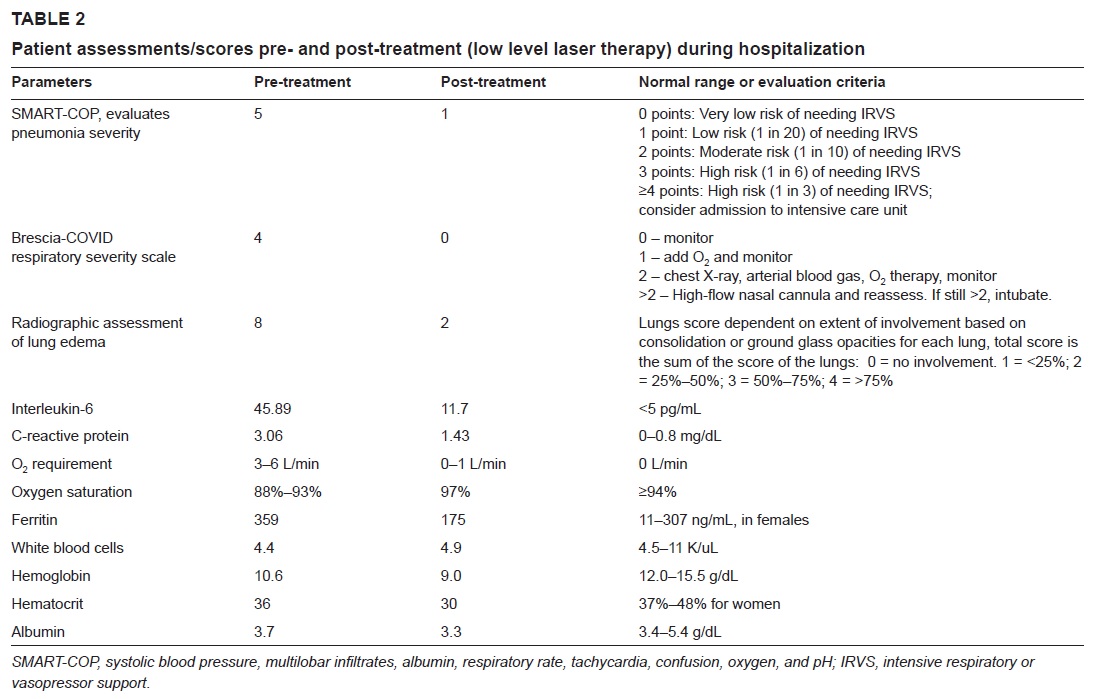
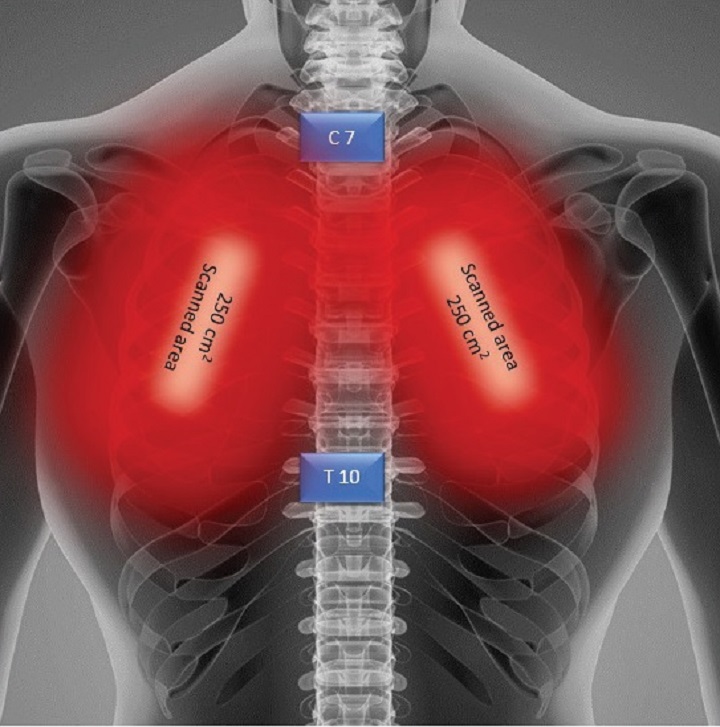
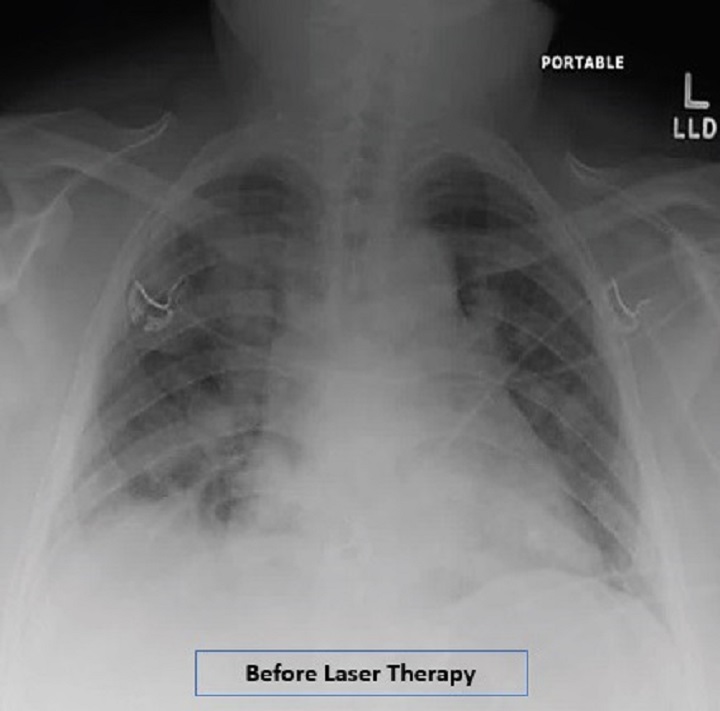
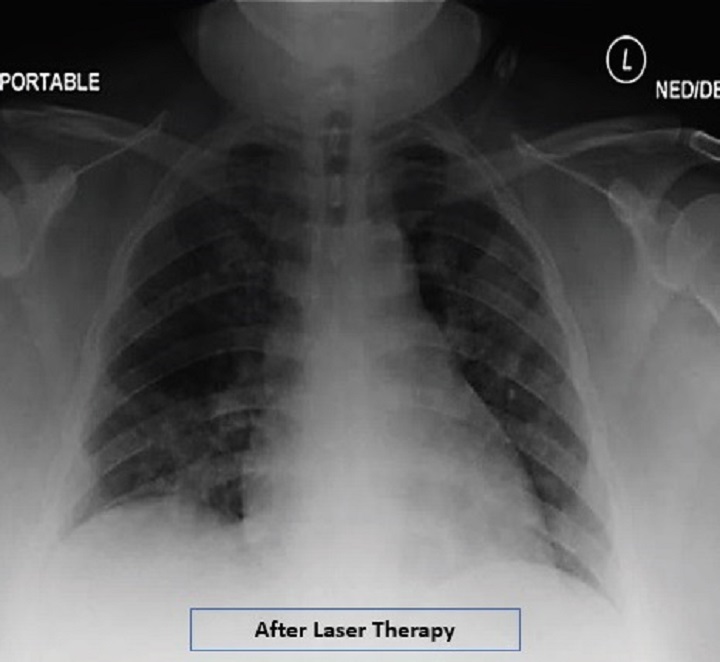
An obese patient with interstitial pneumonia who was treated for 4 days with MLS® Laser Therapy reported a concrete and progressive improvement in her critical parameters such as oxygen saturation, which increased to 97-99%, radiographic assessment of the pulmonary oedema (RALE) which went from 8 to 2, Brescia-COVID Respiratory Severity Scale (a score which assesses the gravity of the pneumonia and is used for patient progress management) which went from 4 to 0 and SMART-COP (a tool which monitors the seriousness of the pneumonia and predicts the need for intervening such as with a move to intensive care, etc.) which dropped from 5 to 1. Interleukin-6, ferritin and C-reactive protein also recorded a significant contraction.
The data were reported by the study “Adjunct low level laser therapy (LLLT) in a morbidly obese patient with severe COVID-19 pneumonia: A case report” whose conclusions indicate that use of MLS® Laser Therapy for the case in question recorded a significant improvement of the respiratory indexes, radiological results and inflammatory markers in just a few days.
A result which suggests that ASA’s therapy can safely be combined with conventional treatment for patients suffering from severe COVID-19 and morbid obesity.