MLS® e COVID-19: nuovo successo nel trattamento della polmonite interstiziale
02 Ottobre 2020 - Ricerca -
Condividi
Un nuovo caso conferma l’efficacia di MLS® come terapia di supporto nel trattamento di polmonite causata da COVID-19.
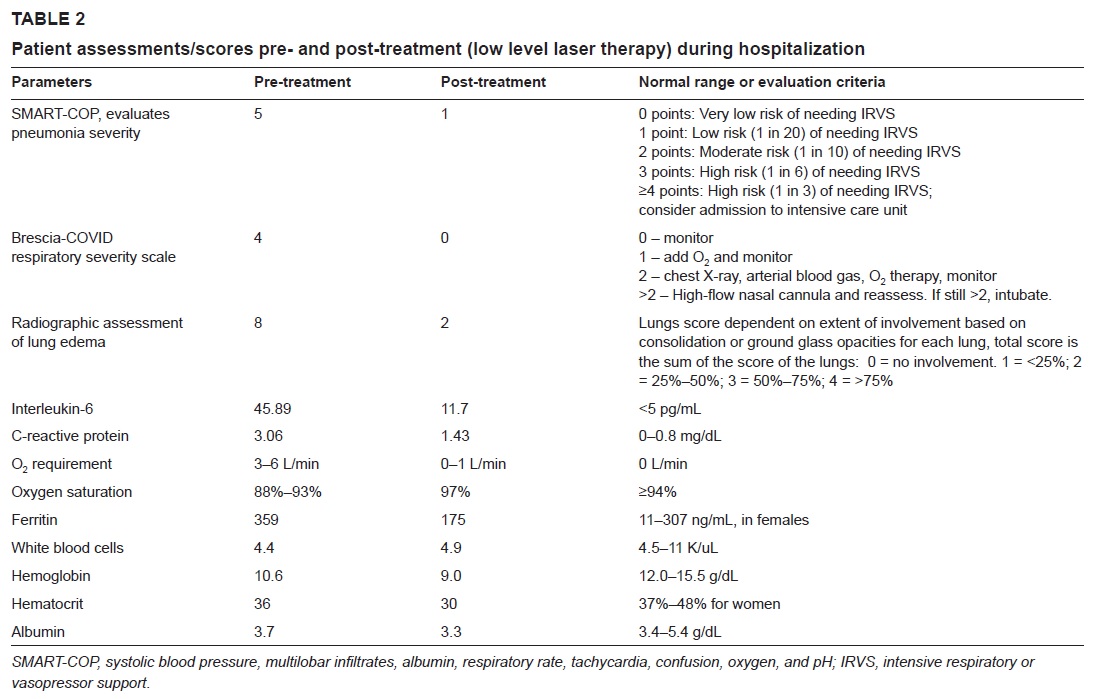
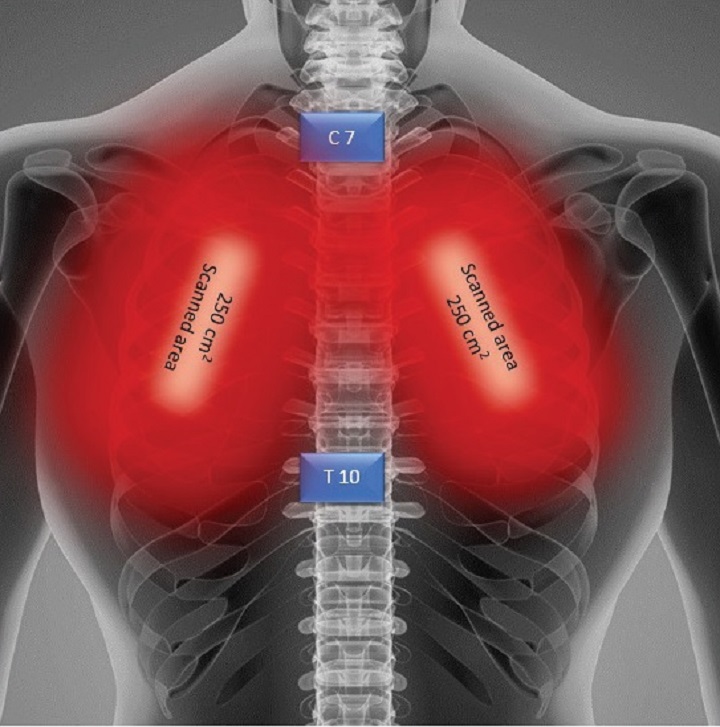
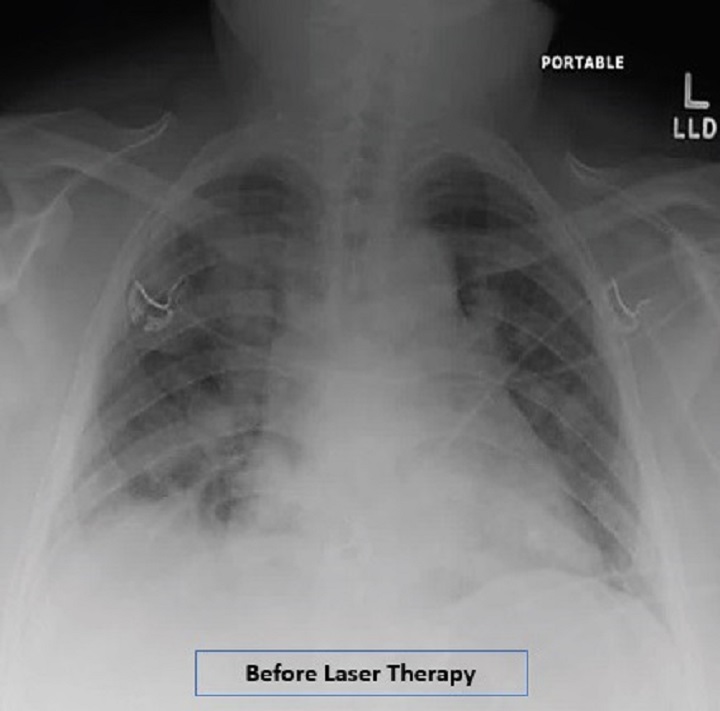
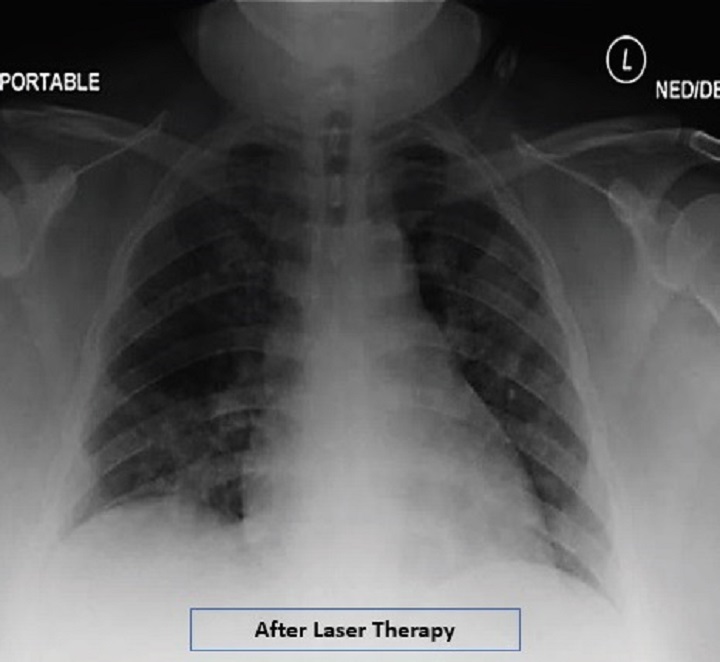
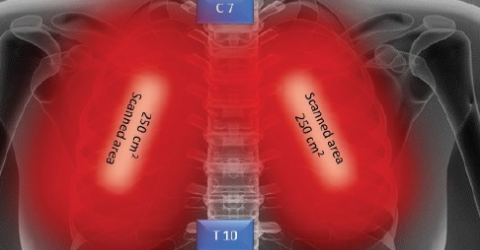
Una paziente obesa con pneumonia interstiziale, trattata per 4 giorni con Laserterapia MLS®, ha visto concretamente e progressivamente migliorare parametri critici come la saturazione di ossigeno, aumentata al 97-99%, la valutazione radiografica dell’edema polmonare (RALE) ridottasi da 8 a 2, il Brescia COVID (punteggio che valuta la gravità della polmonite e serve per la gestione a step dei pazienti) diminuito da 4 a 0 e lo SMART-COP (valore che monitora la gravità della polmonite e predice la necessità di interventi come ad esempio passaggio in terapia intensiva etc.) passato da 5 a 1. Anche l’interleuchina-6, la ferritina e la proteina C reattiva hanno registrato una sensibile contrazione.
A riportare i dati è lo studio “Adjunct low level laser therapy (LLLT) in a morbidly obese patient with severe COVID-19 pneumonia: A case report” che, nelle conclusioni, indica come l’uso della Laserterapia MLS® nel caso in oggetto abbia fatto registrare, in pochi giorni, miglioramenti negli indici respiratori, nei risultati radiologici e nei marker infiammatori.
Un risultato che suggerisce come la terapia di ASA possa essere combinata in sicurezza con il trattamento convenzionale nei pazienti con grave COVID-19 e obesità patologica.
Max 980px