M6 nella prevenzione della neuropatia periferica causata da chemioterapia: uno studio
04 Aprile 2022 - Ricerca -
Condividi
NEUROLASER è questo il nome del recente studio pilota svolto da un team di ricercatori della facoltà di medicina della Hasselt University in collaborazione con i medici dei dipartimenti di Oncologia e Neurologia del Jessa Hospital (Hasselt, Belgio).
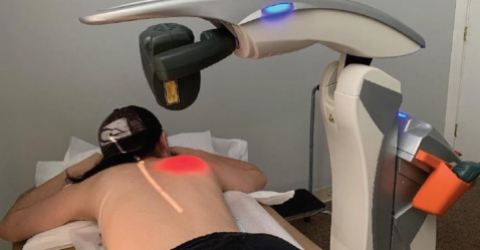
Il trial clinico ha indagato l'efficacia e la sicurezza della terapia di fotobiomodulazione (PBMT) erogata mediante sorgente laser (M6) nella prevenzione della neuropatia periferica indotta da chemioterapia (CIPN) in pazienti con tumore al seno.
Il team guidato dalla Dr.ssa Robijns ha coinvolto nello studio 32 pazienti, di cui 16 sono stati sottoposti a PBMT e 16 a trattamento placebo.
Dai dati raccolti sono emersi risultati promettenti in termini di prevenzione. Sintomi come l’intorpidimento delle mani e dei piedi sono significativamente peggiorati nel gruppo di controllo, mentre sono rimasti costanti nel gruppo trattato con PMB. Anche la qualità della vita nei pazienti trattati è migliorata rispetto ai pazienti del gruppo di controllo. Tutti i trattamenti con laserterapia si sono dimostrati sicuri e privi di effetti indesiderati.
Per confermare l’applicabilità e l’efficacia della terapia laser nella prevenzione delle neuropatie periferiche indotte da chemioterapia sono necessari ulteriori studi, che permetteranno di aumentare la casistica. Tuttavia, questo studio preliminare fornisce risultati incoraggianti sulla possibilità di applicare il sistema M6 nelle terapie di supporto ai pazienti oncologici, come già messo in evidenza da pregresse esperienze legate al trattamento delle radiodermatiti.
Testo a Destra
Immagine 30%/Testo 60%

“The use of photobiomodulation therapy for the prevention of chemotherapy-induced peripheral neuropathy: a randomized, placebo-controlled pilot trial (NEUROLASER trial)”
Supportive Care Cancer, Mar 21;1-9, 2022