MiS Day à Madrid
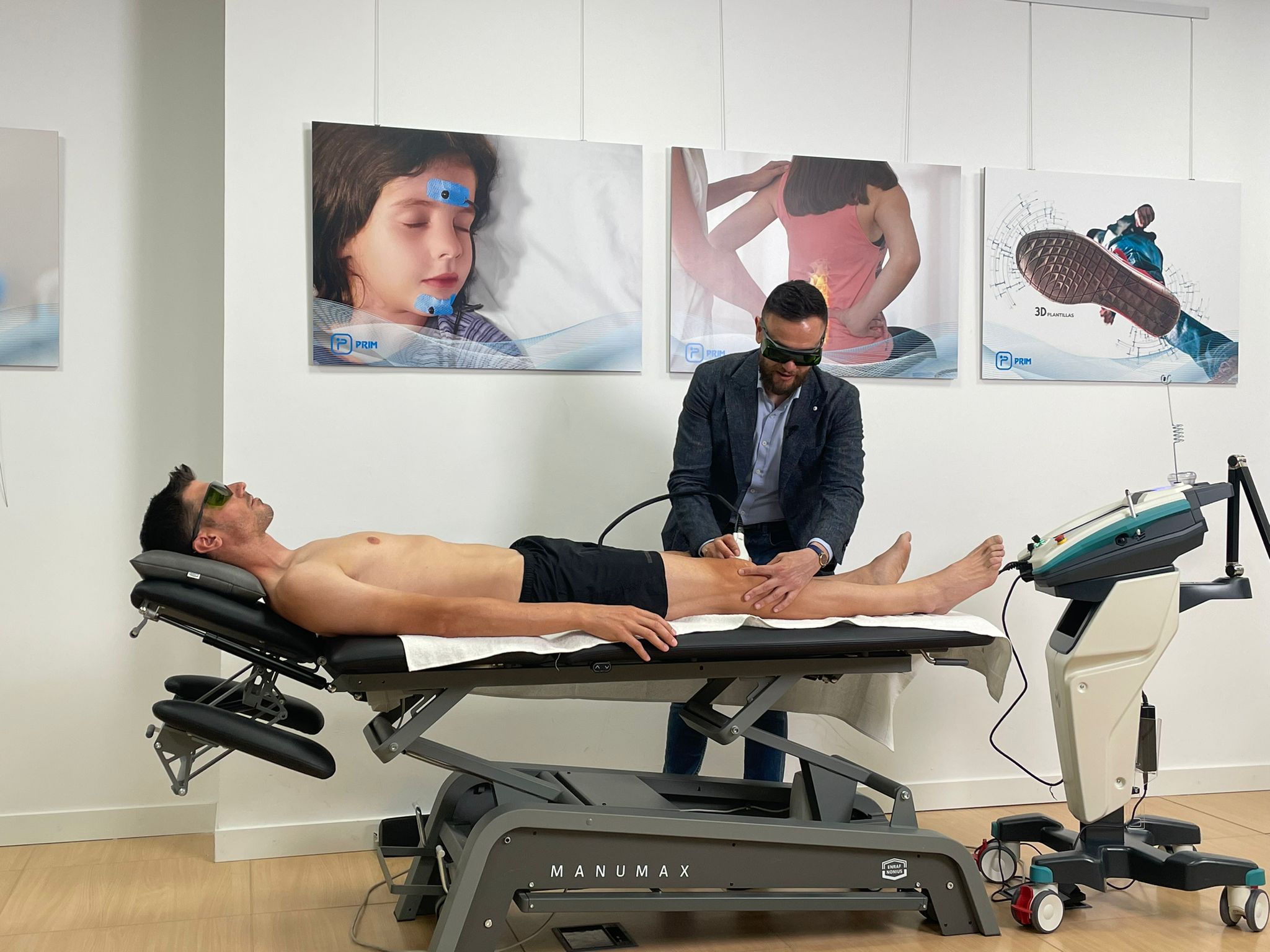
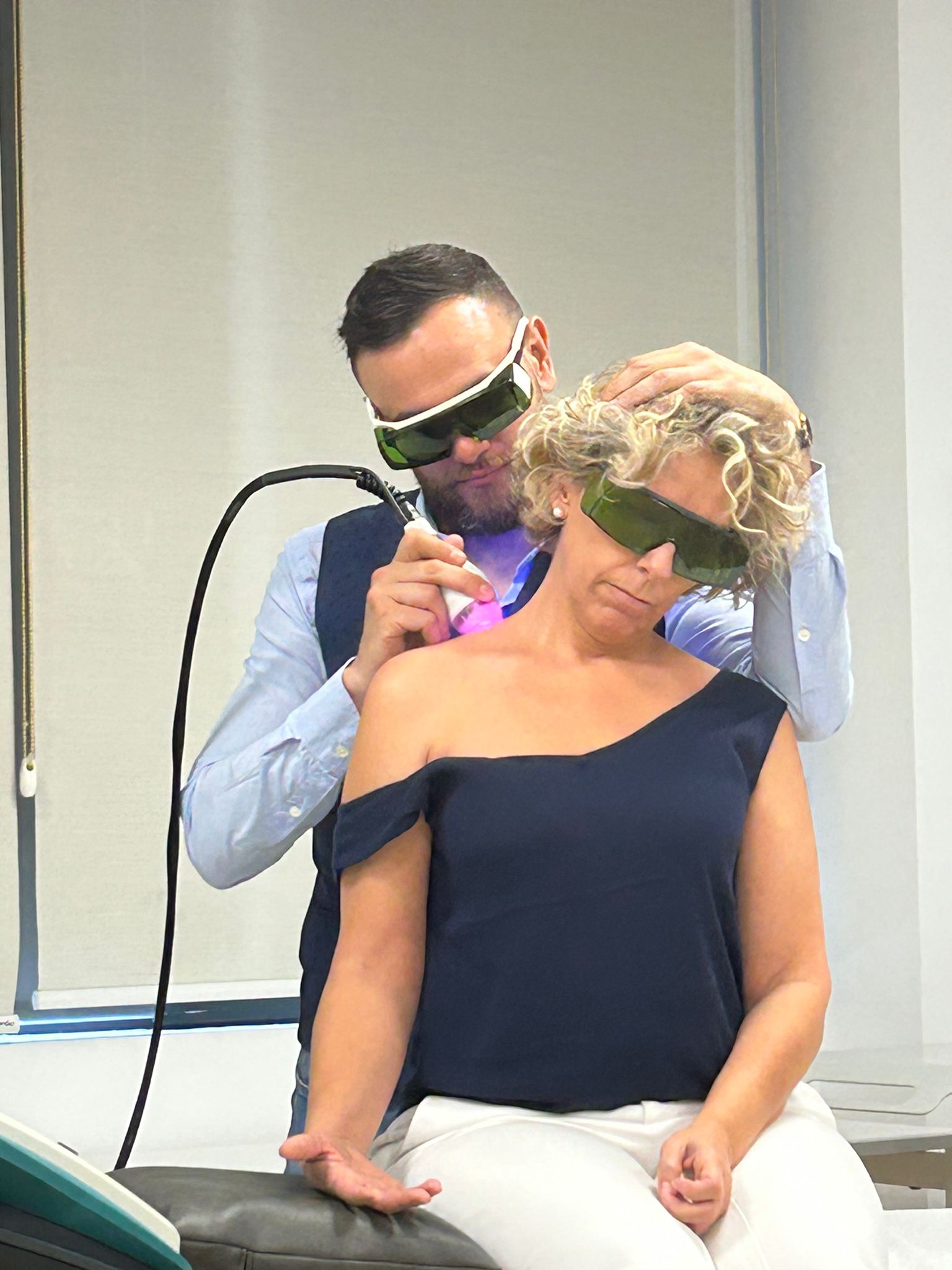
L’objectif du séminaire d’approfondissement dédié au dispositif Mis, organisé par ASA à Madrid, a permis de présenter les options pour le meilleur traitement des neuropathies aux physiothérapeutes et spécialistes de la rééducation montrant un intérêt particulier envers ce sujet. Grâce à la collaboration du distributeur local Prim, dont l’Academy a été le siège du cours à numerus clausus, le staff de l’entreprise a pu mettre l’accent non seulement sur les caractéristiques techniques du dispositif, mais également sur les bienfaits concrets de son application à travers la présentation de cas cliniques ad-hoc.
“Durant le séminaire – explique Cinzia Pacini, Area Manager ASA – notre Specialist Salvatore Germano, soutenu par Giacomo Granozio, Education Program Manager ASA, a montré les modalités d’application de notre solution thérapeutique sur différentes conditions neuropathiques, de manière à fournir des contributions concrètes aux participants quant au caractère unique et aux bienfaits du dispositif dans ce domaine si délicat”.
La formule adoptée s’est avérée gagnante, au point que les matériaux utilisés seront intégrés dans un cours universitaire sous peu.
“Cette invitation atteste de la valeur de notre thérapie, mais représente également une occasion importante pour ouvrir des canaux de collaboration avec les futurs professionnels du secteur », conclut Pacini.