MiS Day in Madrid
26 Juni 2023 - Ausbildung -
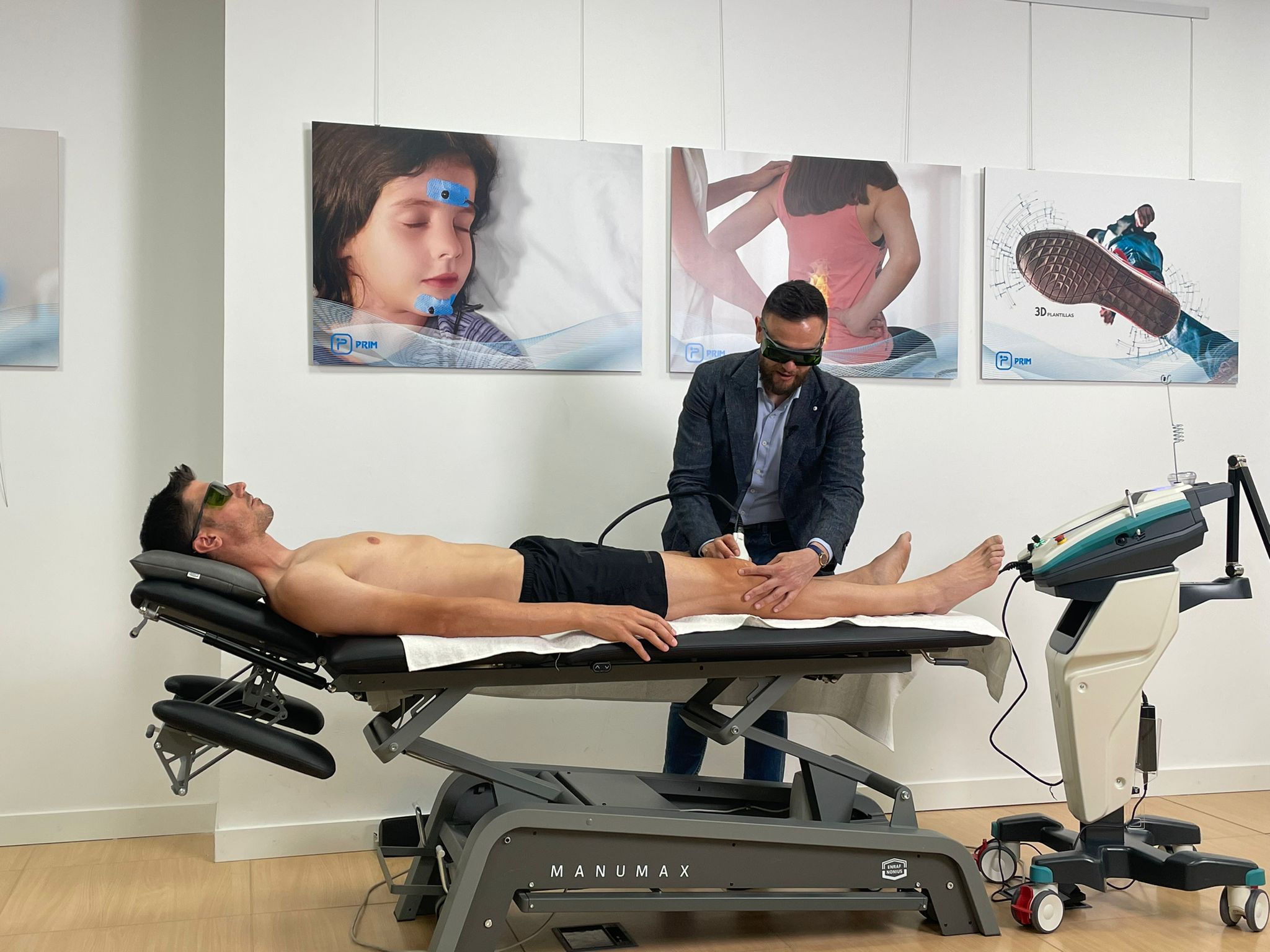
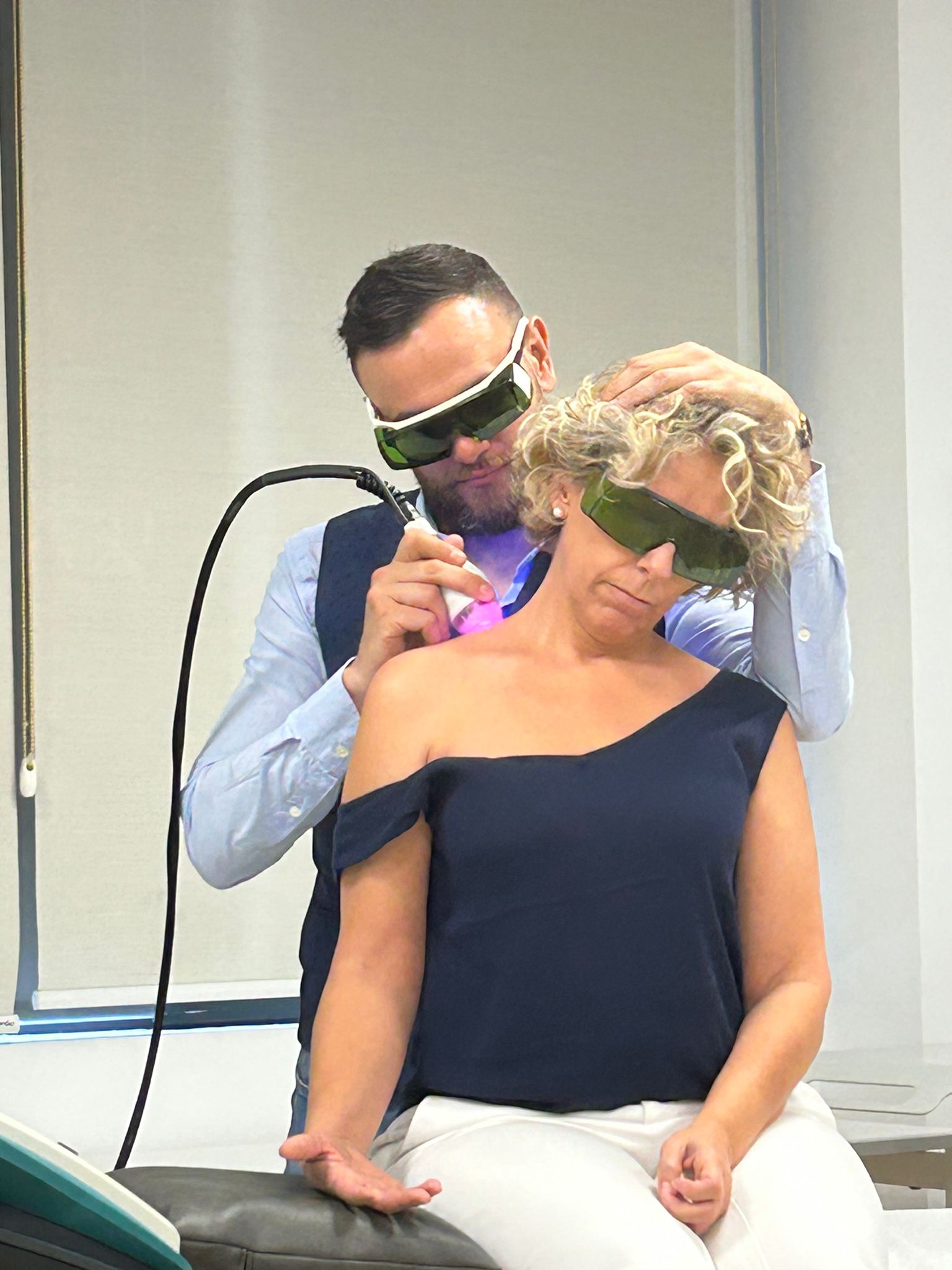
Physiotherapeuten und Rehabilitationsfachleute, die ein besonderes Interesse daran haben, mehr über die Möglichkeiten einer optimalen Behandlung von Neuropathie zu erfahren: Das war die Zielgruppe des von ASA in Madrid organisierten Workshops, der sich eingehend mit dem MiS-Gerät befasste. In Zusammenarbeit mit dem örtlichen Vertriebshändler Prim, in dessen Academy der Kurs mit begrenzter Teilnehmerzahl stattfand, konnten die Mitarbeiter des Unternehmens nicht nur die technischen Merkmale des Geräts erläutern, sondern auch die konkreten Vorteile seiner Anwendung anhand von klinischen Ad-hoc-Fällen aufzeigen.
“Während des Workshops", erklärt Cinzia Pacini, Area Manager ASA, "hat unser Spezialist Salvatore Germano mit Unterstützung von Giacomo Granozio, Education Program Manager ASA, gezeigt, wie unsere therapeutische Lösung bei einer Vielzahl von neuropathischen Erkrankungen angewendet werden kann, um den Seminarteilnehmern konkrete Hinweise auf die Einzigartigkeit und den Nutzen des Geräts in diesem delikaten Bereich zu geben”.
Die gewählte Formel erwies sich als so erfolgreich, dass die verwendeten Materialien in naher Zukunft in einen Universitätskurs integriert werden.
“Diese Einladung ist ein wertvolles Zertifikat für unsere Therapie, aber auch eine wichtige Gelegenheit, Kanäle für die Zusammenarbeit mit zukünftigen Fachleuten in diesem Bereich zu öffnen", so Pacini abschließend.