MLS® und COVID-19: Neuer Erfolg in der Behandlung von interstitieller Pneumonie
02 Oktober 2020 - Forschung -
Share
Ein neuer Fall bestätigt die Wirksamkeit von MLS® als unterstützende Therapie in der Behandlung von Pneumonien infolge von COVID-19.
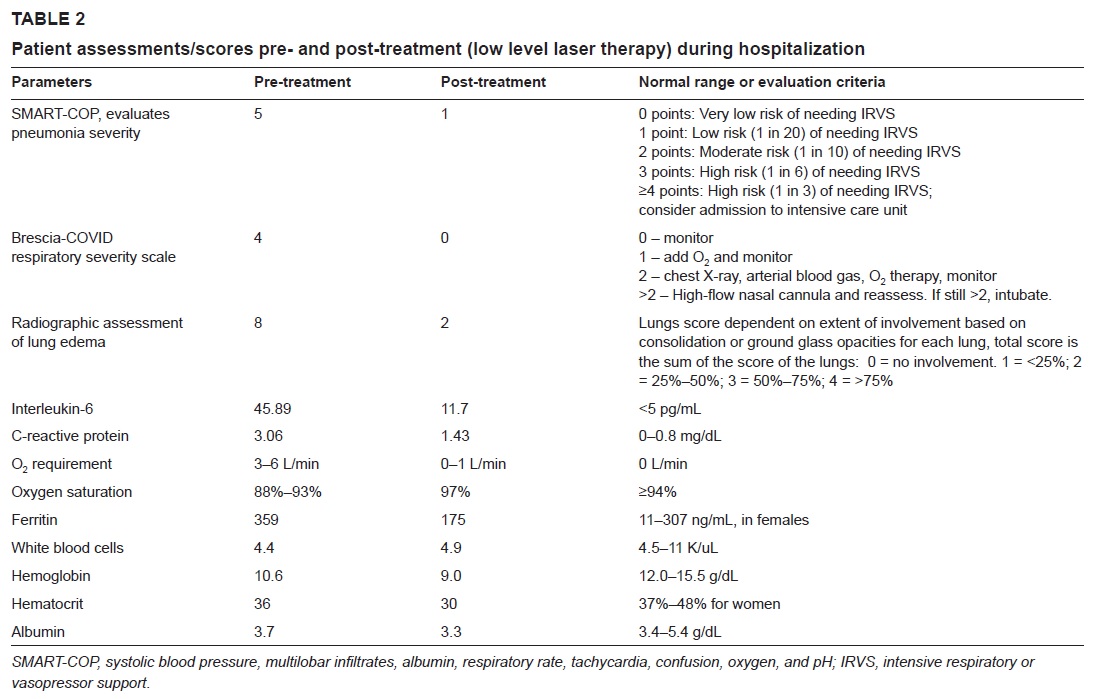
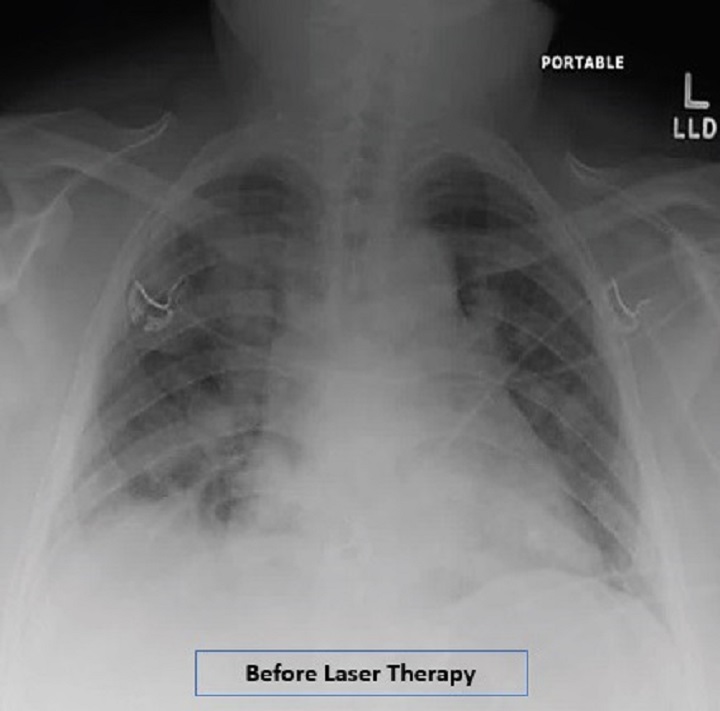
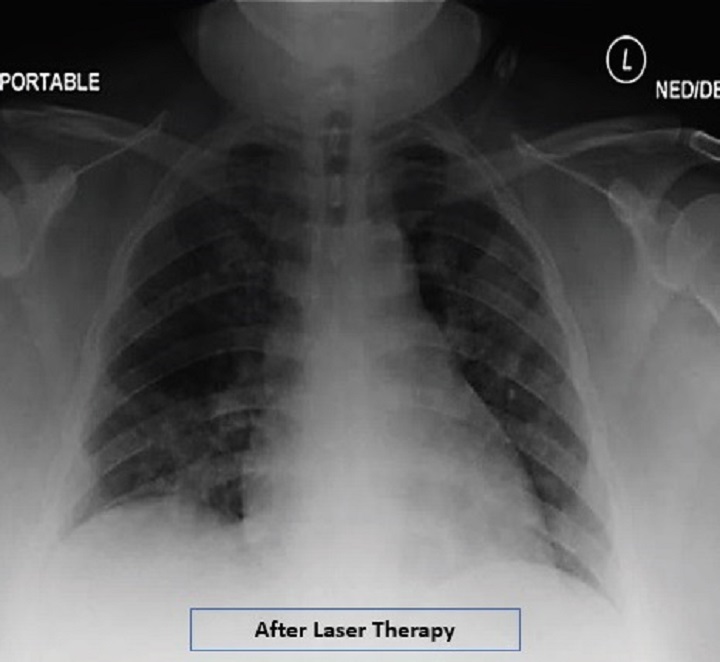
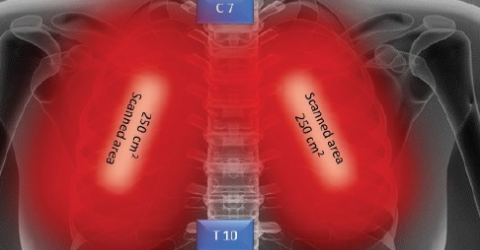
Eine übergewichtige Patientin mit interstitieller Pneumonie, die vier Tage lang mit der MLS®-Lasertherapie behandelt wurde, zeigte eine konkrete und schrittweise Besserung kritischer Parameter wie die Sauerstoffsättigung, die um 97-99 % gestiegen ist, die Röntgenuntersuchung des Lungenödems (RALE), die eine Reduktion von 8 auf 2 ergab, der Index Brescia-COVID (Punktewertung, mit der die Schwere der Pneumonie eingestuft wird und die zur schrittweisen Behandlung der Patienten dient), der sich von 4 auf 0 verringerte, und der Score SMART-COP (Wert, mit dem die Schwere der Pneumonie überwacht und die Notwendigkeit weiterer Behandlungsschritte wie etwa der Übergang zur Intensivtherapie usw. vorhergesagt wird), der von 5 auf 1 zurückging.
Auch für Interleukin-6, Ferritin und das C-reaktive Protein konnte ein leichter Abfall beobachtet werden.
Diese Daten stammen aus der Studie “Adjunct low level laser therapy (LLLT) in a morbidly obese patient with severe COVID-19 pneumonia: A case report” die zusammengefasst darauf hinweist, dass die Anwendung der MLS®-Lasertherapie in diesem Fall innerhalb weniger Tage zu Verbesserungen des respiratorischen Quotienten, der radiologischen Ergebnisse und der Entzündungsmarker führte.
Ein Ergebnis mit dem bewiesen wird, dass die Therapie von ASA auf sichere Weise mit der herkömmlichen Behandlung bei einem schweren Verlauf von COVID-19 und krankhaftem Übergewicht kombiniert werden kann.
Max 980px