Taipei: convegno web & live per MLS®
17 Novembre 2020 - Fiere & Congressi -
L’emergenza COVID-19 e le pratiche di distanziamento imposte non fermano le iniziative di ASA e dei suoi distributori che, grazie alla formula mix “on site” e “on line”, continuano a svolgere meeting di approfondimento sulle soluzioni terapeutiche dell’azienda.
Ultimo in ordine temporale è stato il convegno “Taipei MLS® User Meeting” svoltosi al Caesar Park di Taipei grazie alla collaborazione con il partner locale Gaia Genomics.
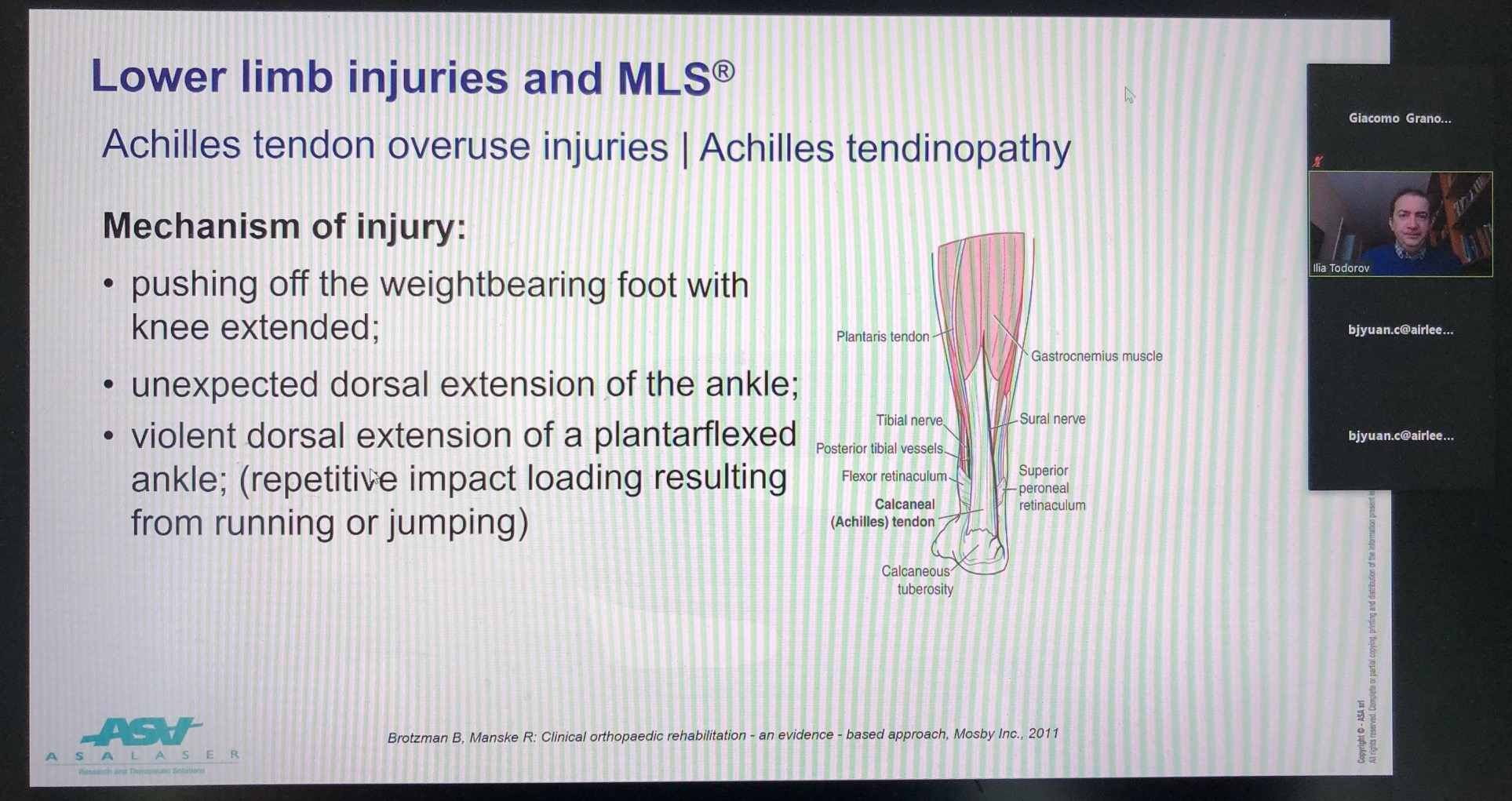
L’incontro ha visto la presenza fisica di 4 specialisti del settore fisioterapico e riabilitativo chiamati a condividere le loro esperienze cliniche nell’utilizzo dei dispositivi M6 e Mphi 75 e, da remoto, il contributo del Dr. Iliya Todorov, Direttore del Comitato Educativo per la Federazione Internazionale di Medicina Manuale-Muscoloscheletrica e Presidente della Società Bulgara di Medicina Manuale-Muscoloscheletrica.
Suo il compito di mettere l’accento sull’utilizzo di MLS® nel trattamento delle patologie degli arti inferiori attraverso numerosi casi clinici.
Tre i punti su cui si sono concentrate le domande dei partecipanti al Dr. Todorov per meglio comprendere il valore della terapia:
- quanto MLS® velocizza il recupero rispetto a tempistiche standard;
- la possibilità di usare la Laserterapia MLS® con efficacia nel post-chirurgico;
- quando è suggeribile iniziare a trattare un paziente che presenta una lesione muscolare o tendinea.
“L’interazione tra i partecipanti e il relatore è stata utile per rispondere alle domande in diretta – spiega Giacomo Granozio, Export Area Manager ASA – permettendo lo scambio di punti di vista e di esperienze sul campo”. Della stessa opinione lo stesso Todorov che sottolinea come questo meeting sia stato “una grande opportunità per condividere conoscenze e opinioni con i medici locali” e si augura che “i casi mostrati saranno utili per la loro pratica quotidiana”. Ne è convinta Celine, CEO di Gaia Genomics: “Il discorso del Professore ha avuto un forte impatto sui partecipanti che, dopo la sua presentazione, si sono mostrati convinti dei reali benefici di MLS®”.