La formation Asa pour Formateurs: 3 jours de formation continue
Le début du mois d’avril a été marqué par trois jours de formation réservés aux formateurs ASA de la zone latino-américaine et espagnole directement au quartier général de l’entreprise.
Les rencontres, auxquelles ont participé Monica María Abarca Ulate, Andrés Castañon Mora et Cesar Castaño, ont été caractérisées non seulement par des sessions théoriques centrées sur Hilterapia®, Thérapie Laser MLS® et Magnétothérapie Qs, étayées par des études cliniques ad-hoc, mais aussi par des approfondissements consacrés à certains des dispositifs de pointe comme HIRO TT et MiS.
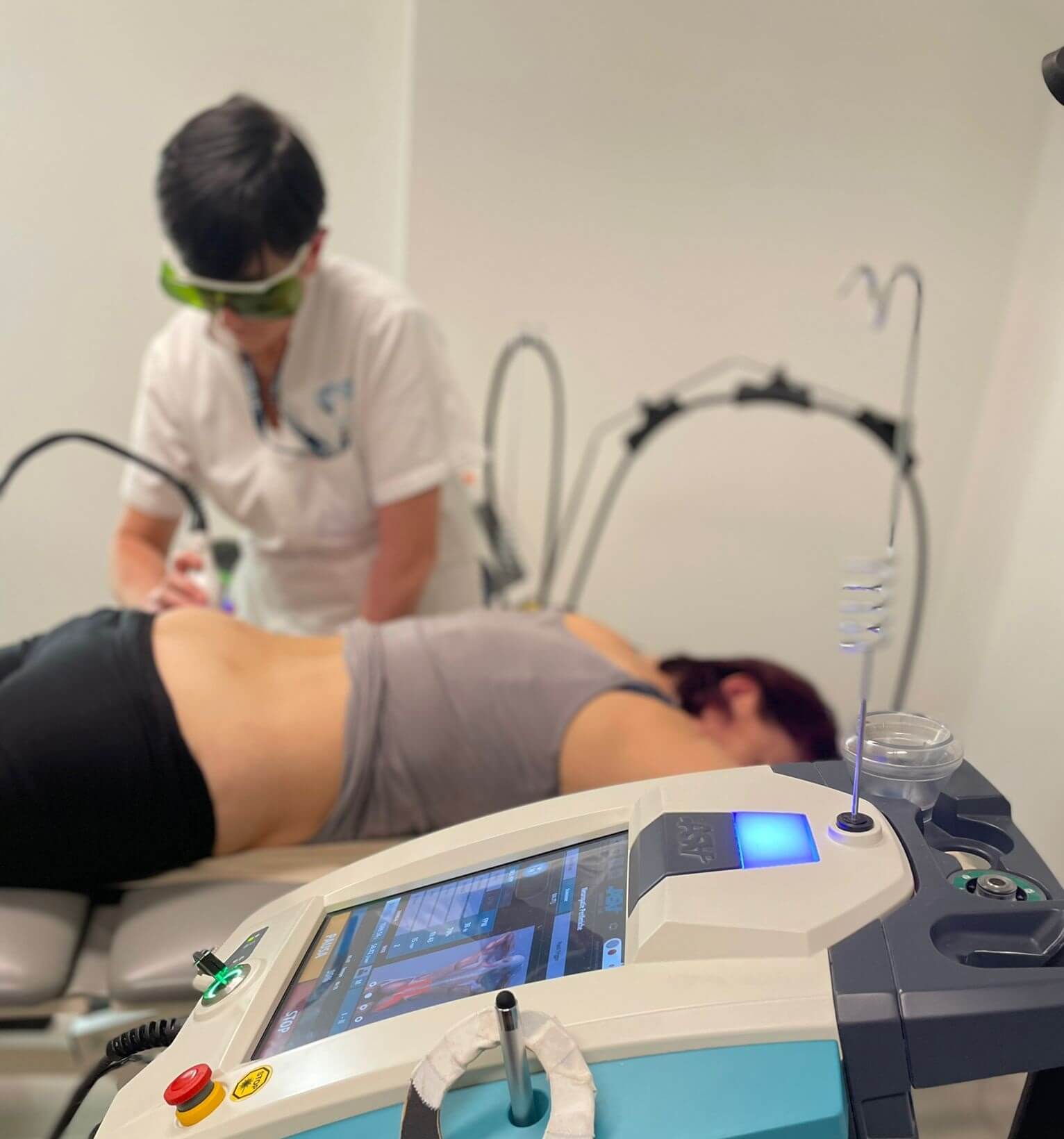
“La partie pratique, réalisée grâce au soutien de plusieurs centres de physiothérapie dotés depuis longtemps de nos dispositifs, s’est avérée particulièrement importante ; elle a permis aux participants de vérifier concrètement l’efficacité des thérapies et la technologie à l’avant-garde de nos systèmes», commente Cinzia Pacini, EMEA Sales Manager ASA.
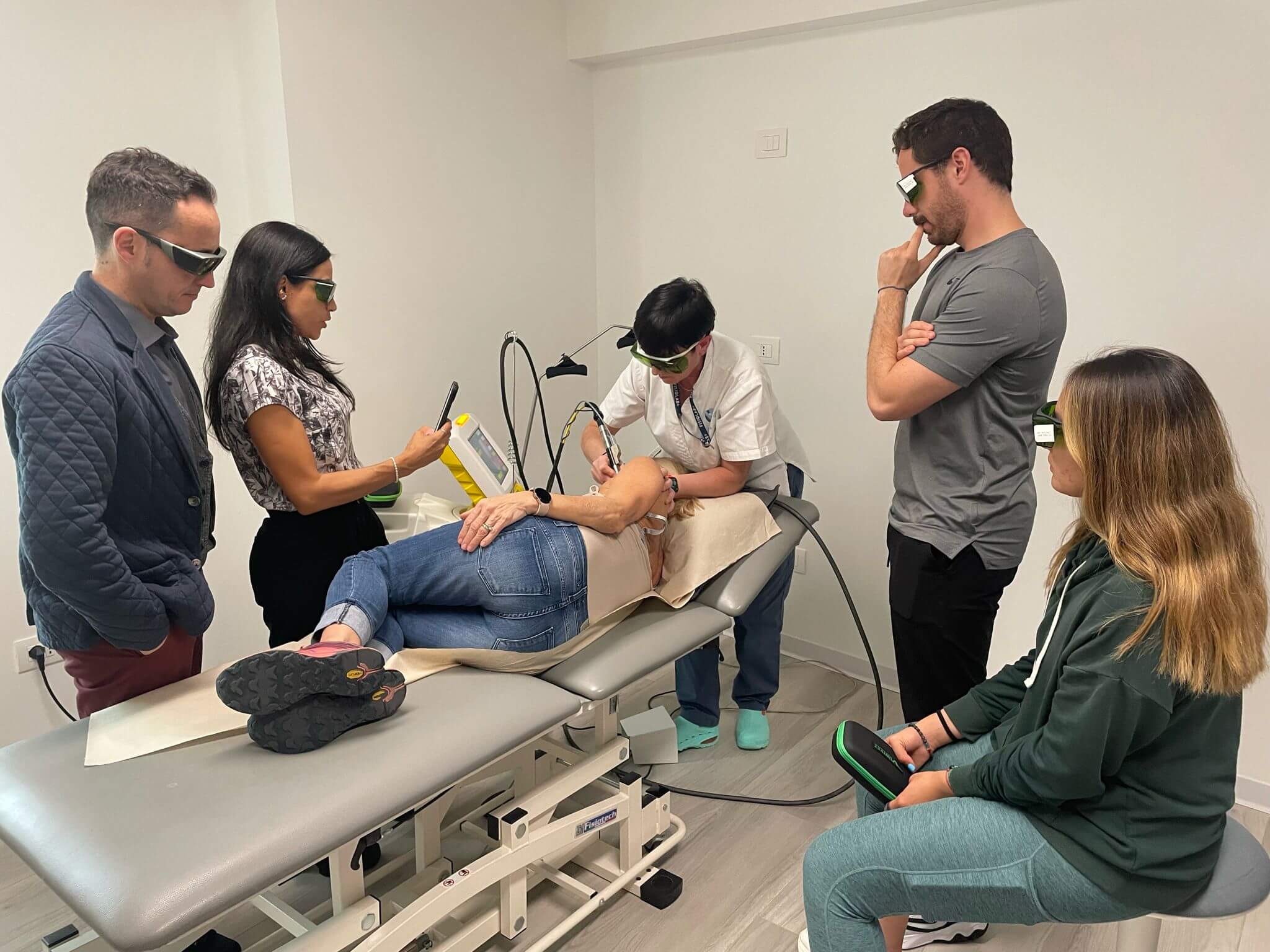
“Les objectifs que nous nous étions fixés avec ce parcours, c’est-à-dire recycler nos formateurs sur les technologies ASA, en leur fournissant toutes les nouveautés en matière de recherches et preuves scientifiques – précise Karla Salazar, Area Manager ASA – ont été amplement atteints. Dans le même temps, ces journées sur le terrain ont également permis aux présents de partager leurs différentes expériences et d’acquérir ainsi de nouvelles connaissances en créant une équipe soudée”.