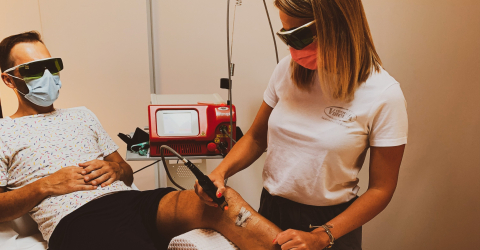
Formation Hilterapia® en présentiel pour trois cliniques espagnoles
Fournir des informations précises sur les caractéristiques de Hilterapia®, sur ses bienfaits tangibles et, en même temps, donner des indications pour la meilleure utilisation de Hiro 3.0 au personnel de différentes cliniques espagnoles du groupe Asepeyo: c’est en poursuivant cet objectif que l’équipe ASA s’est activée pour soutenir le distributeur local Prim dans une activité de formation qui s’est tenue à plusieurs reprises, initialement, en distanciel, et seulement récemment en présentiel.
“Des sessions de formation en ligne ont initialement été prévues afin d’optimiser le parcours de formation – explique Roberto Terruzzi, Senior Area Manager ASA – celles-ci incluaient une première introduction théorique sur la thérapie. Par la suite on a organisé une intervention en présentiel destinée à tout le personnel du service de physiothérapie des cliniques de Madrid et Barcelone faisant partie du groupe Asepeyo. Ces deux équipes ont été rejointes par celle de la structure de Marbella qui, comme les deux autres, dispose d’un dispositif Hiro 3.0”.





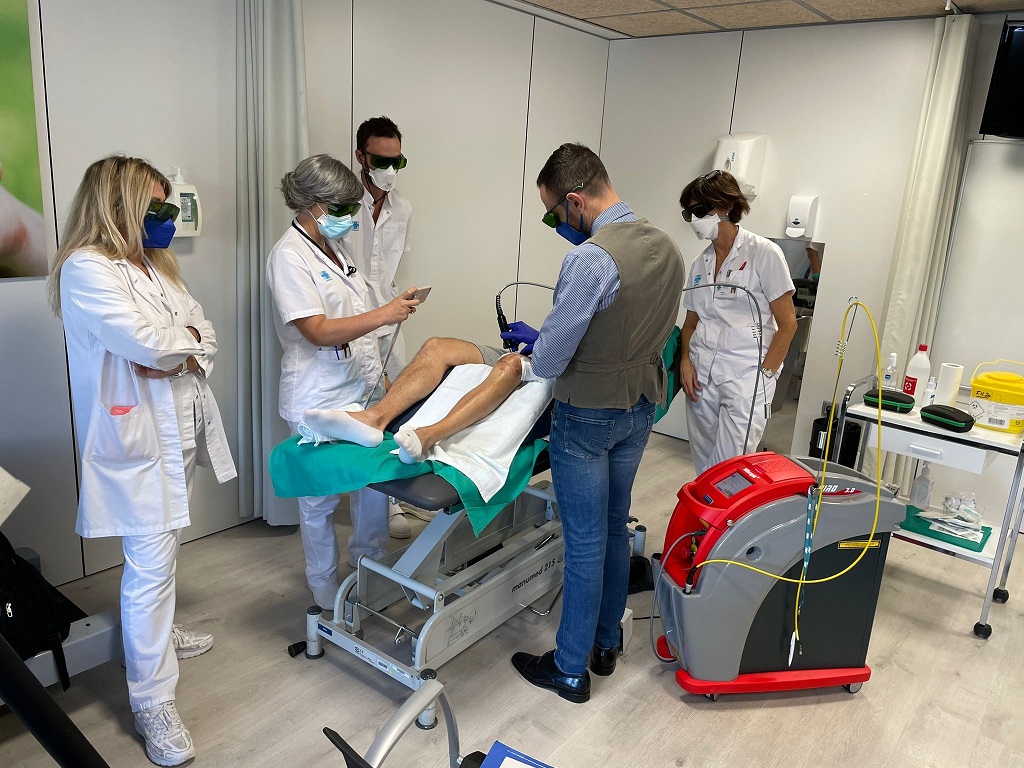
Des retours positifs significatifs ont été recueillis à la fin du cours, auquel tous les présents ont participé activement.
“Les nombreuses questions qui nous ont été posées, surtout sur la manière d’améliorer l’emploi de Hilterapia® au quotidien dans le traitement de pathologies spécifiques et de mener au mieux des séances thérapeutiques n’ont fait que confirmer l'intérêt des physiothérapeutes”.