Thérapie Laser MLS® et paralysie de Bell: une étude sur son efficacité
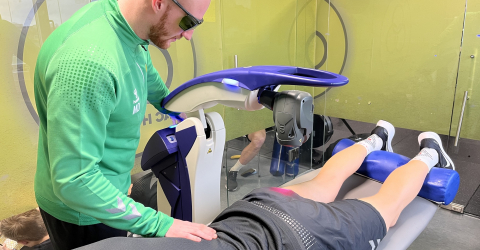
Une étude publiée sur Lasers in Medical Science s’est penchée sur l’efficacité de la Thérapie Laser MLS® chez des patients atteints de la paralysie faciale unilatérale aiguë grâce au dispositif robotisé M6.
Paralysie de Bell: de quoi s’agit-il?
- La paralysie de Bell est la cause la plus commune de paralysie faciale unilatérale aiguë, avec une incidence moyenne de 15-30 cas sur 100 000.
- Elle est causée par une dysfonction du nerf facial, le VII nerf crânien. Ce nerf est responsable de l’innervation de tous les muscles du visage servant à la mimique faciale.
- La paralysie de Bell détermine une faiblesse marquée des muscles faciaux d’un côté du visage, outre: l’asymétrie du sourire causée par le coin de la bouche qui tombe, l’impossibilité de fermeture palpébrale, la disparition des rides du front, la diminution de la stimulation des glandes lacrymales et salivaires.
- Les symptômes se manifestent soudainement – le pic maximum s’atteint en à peine 72 heures – et sont généralement asymptomatiques.
- Les médicaments utilisés généralement sont les corticostéroïdes – pour réduire l’inflammation et le gonflement – et les analgésiques pour traiter la douleur.
- La physiothérapie – surtout si commencée durant les premières 72 heures après l’apparition des symptômes – est fondamentale pour stimuler le nerf facial et l'aider à maintenir un bon tonus musculaire.
L’étude
“Effectiveness of multiwave locked system laser on the treatment of patients with idiopathic Bell's palsy: a randomized double-blind placebo controlled trial.» est une recherche spontanée récente publiée sur Lasers in Medical Science [vol. 37,9 (2022):3495-3502] visant à analyser le traitement de patients atteints de la paralysie de Bell en exploitant les caractéristiques du dispositif robotisé M6 pour Thérapie Laser MLS®. Même si la publication en question se distingue pour être randomisée, en double aveugle, contrôlée et prospective, ce domaine d’application est encore en phase d’approfondissement et d’étude.
Plus précisément, les 60 patients inclus ont été divisés en 3 groupes:
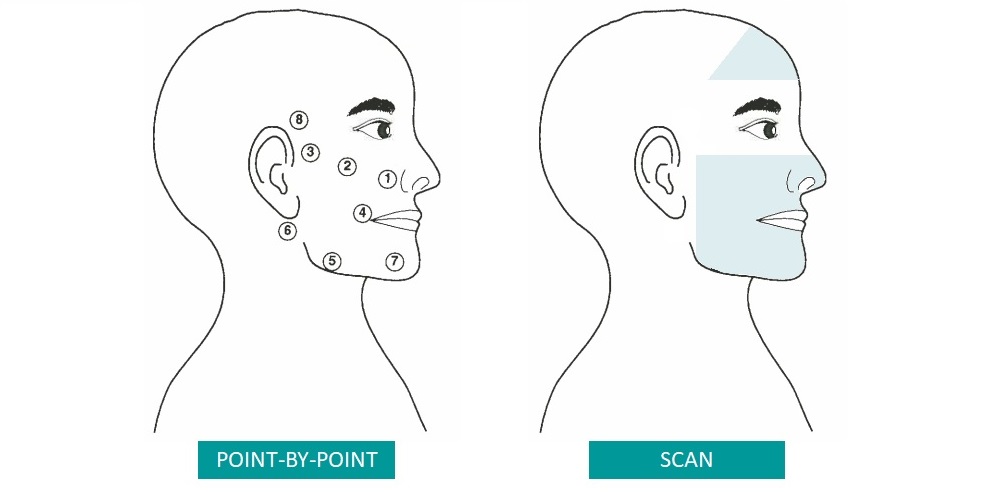
- Groupe A – MLS® par balayage + massages + exercices
- Groupe B – MLS® par points + massages + exercices
- Groupe C – Sham-Laser (laser simulé) + massages + exercices
Le cycle de traitement a prévu 2 séances par semaine pendant 6 semaines.
Chaque patient a été évalué à la visite initiale, à mi-parcours (après 3 semaines et 6 séances) et à la fin du cycle de traitement (après 6 semaines et 12 séances).
Pour mesurer les effets de la thérapie on a eu recours à la House-Brakman Scale (HBS) et au Facial Disability Index (FDI), constitué de deux sous-échelles : le Physical Facial Disability Index (PFDI) et le Social Facial Disability Index (SFDI).
Les résultats
Les résultats ont souligné combien la Thérapie Laser MLS®, en combinaison avec massage et exercice facial, permet une amélioration significative à la fin du cycle de traitement, par rapport à la visite initiale.
Déjà après 6 séances – à la moitié du cycle de traitement – les patients traités avec MLS® aussi bien en mode par balayage que par points ont présenté une amélioration significative en termes de comportement moteur et social ( Facial Disability Index) et degré de paralysie du nerf facial (House–Brackmann Scale).
Lorsque comparée au groupe témoin (Sham-Laser), la Thérapie Laser MLS® a montré une supériorité importante. En particulier, l’application par balayage a montré un effet significatif tant par rapport au groupe témoin que par rapport à l’application par points.