Pneumonie de Covid-19 et MLS®: une histoire de cas réussie
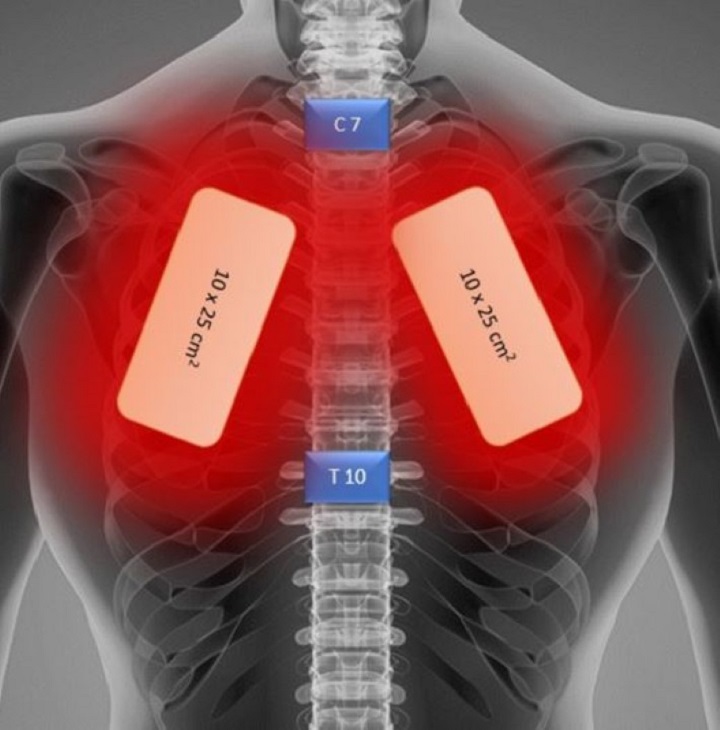
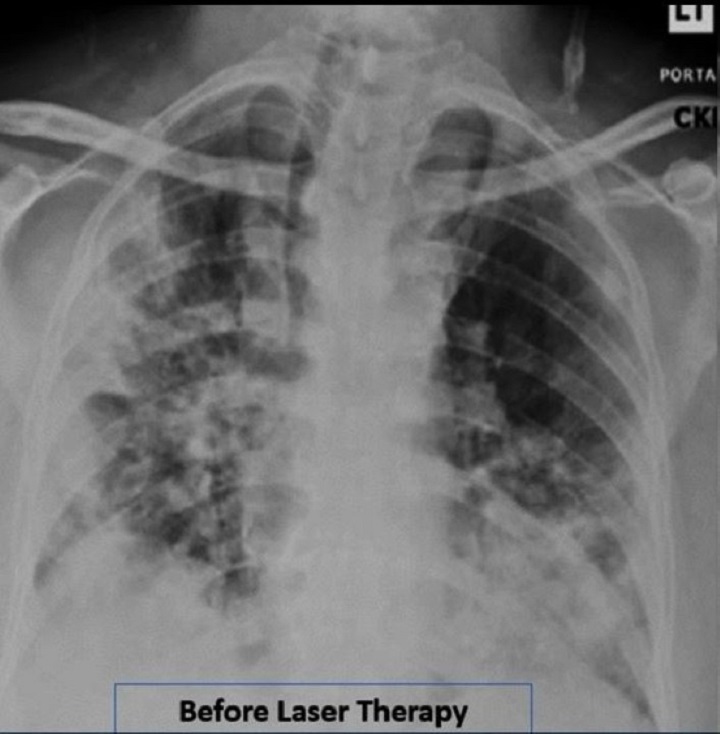
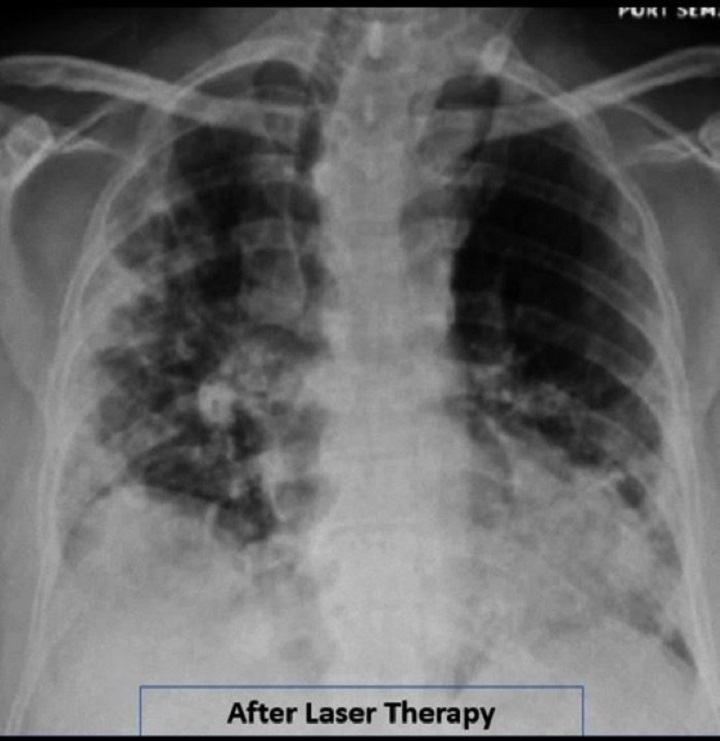
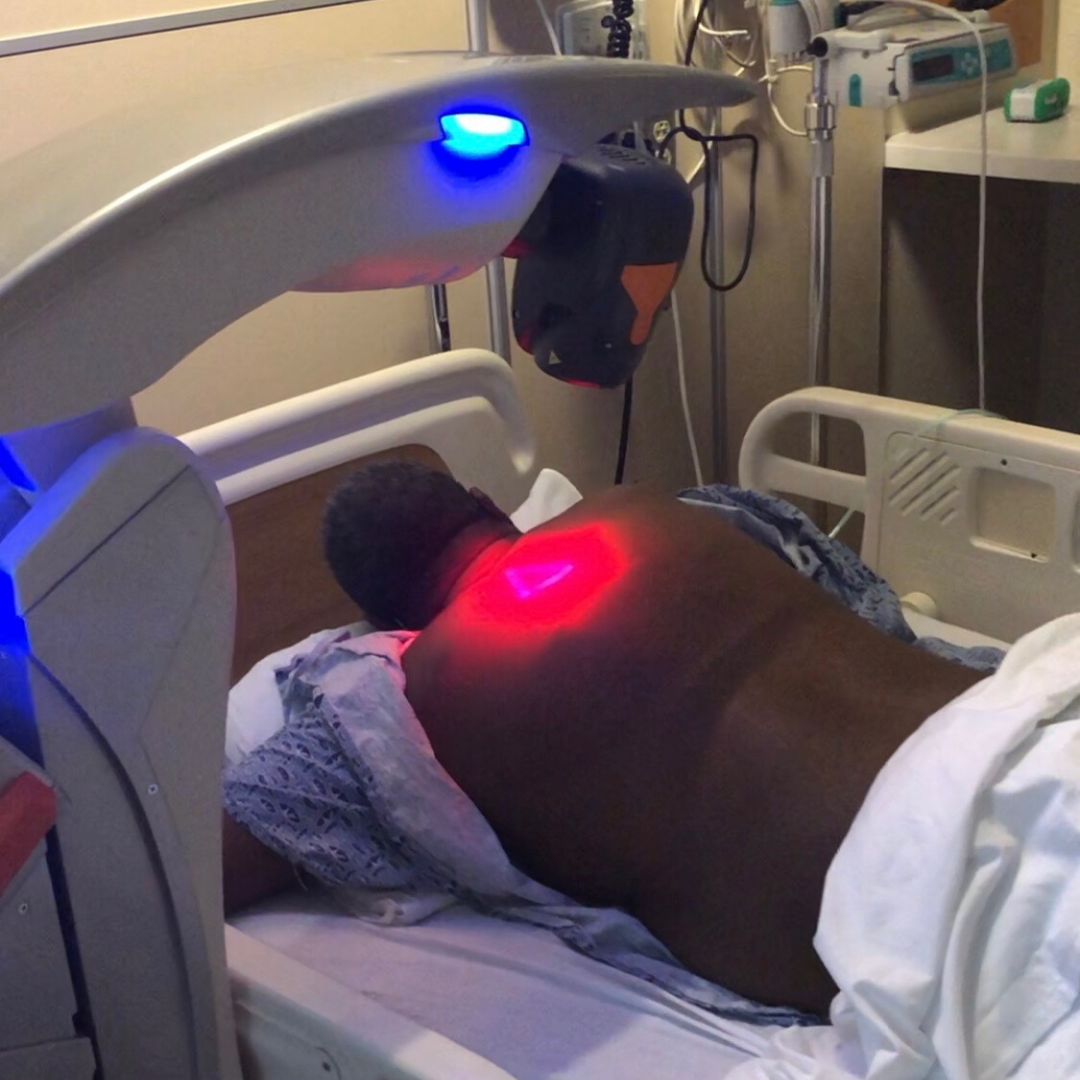
Un rapport de cas très récent consacré à l'utilisation de la thérapie laser MLS® pour soutenir un patient souffrant d'une pneumonie grave causée par Covid-19 – A 57-Year-Old African American Man with Severe COVID-19 Pneumonia Who Responded to Supportive Photobiomodulation Therapy (PBMT): First Use of PBMT in COVID-19 – a fait état d'une amélioration significative de certains paramètres de base (indices respiratoires, résultats radiologiques, besoins en oxygène) pendant plusieurs jours et sans qu'un ventilateur soit nécessaire.
Bien que de futurs essais cliniques contrôlés soient nécessaires pour évaluer les effets de la thérapie laser sur les résultats cliniques chez des patients présentant une pathologie similaire, le cas signalé est significatif, surtout si on entre dans le détail des valeurs monitorées.
Les résultats
Traité quotidiennement pendant 4 jours avec la thérapie MLS®, le patient a en effet enregistré une augmentation de la saturation de 93-94% à 97-100%, une diminution de la demande en oxygène (le débit délivré est passé de 2-4 L/min à 1 L/min) et une contraction d'autres paramètres respiratoires (Brescia-COVID et SMART-COP) de 4 à 0. Par ailleurs, la protéine C-réactive s'est normalisée de 15.1 à 1.23 et le CAP tool score (questionnaire évaluant les symptômes respiratoires et le bien-être) s'est considérablement amélioré.