




ASA bemüht sich ständig um die Verbreitung von Wissen, Forschungsergebnissen und Entdeckungen auf medizinischem und technologischem Gebiet im Zusammenhang mit Lasertherapieanwendungen. Dazu gehört eine von Forschern der Universität Kairo durchgeführte Studie mit dem Titel: "Effect of high-intensity laser therapy on the range of motion of facial muscles in patients with Chronic Bell's Palsy" (Auswirkung der Hochintensitäts-Lasertherapie auf den Bewegungsumfang der Gesichtsmuskeln bei Patienten mit chronischer Bell-Lähmung), veröffentlicht in SPORT TK-Revista Euro Americana de Ciencias del Deporte.
Die Studie untersuchte die Auswirkungen der Hilterapia® bei Patienten mit Bell-Lähmung.
Die Bell-Lähmung ist eine idiopathische, überwiegend einseitige Form der Gesichtslähmung, die in etwa 15-30 Fällen pro 100 000 Menschen auftritt.
Sie ist gekennzeichnet durch eine Funktionsstörung des Gesichtsnervs (7. Hirnnerv), der für die Innervation der an der Mimik beteiligten Muskeln verantwortlich ist. Das plötzliche Auftreten der Symptome, die bereits nach 72 Stunden ihren Höhepunkt erreichen können, führt zu Gesichtsschwäche, herabhängenden Mundwinkeln, der Unfähigkeit, die Augenlider zu schließen, und anderen Asymmetrien im Gesicht. Zu den gängigen Behandlungsmöglichkeiten gehören Kortikosteroide zur Verringerung der Entzündung und Physiotherapie zur Stimulierung des Gesichtsnervs.
Forscher der Universität Kairo führten eine Studie durch, um die Auswirkungen von Hilterapia® auf die Beweglichkeit der Gesichtsmuskeln bei Patienten mit chronischer Bell-Lähmung (≥ 6 Monate) zu untersuchen. An der Studie nahmen 40 Personen im Alter zwischen 20 und 40 Jahren teil, von denen 20 an einer Bell-Lähmung litten und 20 gesunde Personen die Kontrollgruppe bildeten.
Mit Hilfe von 20 radiologischen Hautmarkern an bestimmten Orientierungspunkten und einer ausgefeilten CAD-Bildverarbeitung maß das Ärzteteam den Bewegungswinkel von fünf verschiedenen Gesichtsmuskeln auf beiden Seiten des Gesichts bei vordefinierten Gesichtsbewegungen und -ausdrücken.
Die Patienten mit Bell-Lähmung wurden einmal wöchentlich in insgesamt vier Sitzungen mit dem HIRO 3.0-Gerät mit Hilterapia® behandelt.
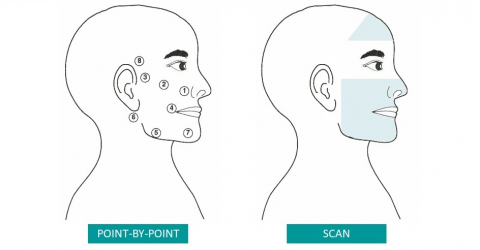
Die Hilterapia®-Sitzungen umfassten drei Phasen: schneller Scan, Triggerpunkt und langsamer Scan, mit einer Gesamtbehandlungsdauer von 15 Minuten.
Darüber hinaus wurden die Patienten angewiesen, zwischen den Sitzungen einfache Gesichtsübungen durchzuführen.
Am Ende des Behandlungszyklus stellten die Forscher deutliche Verbesserungen fest. Die Bewegungswinkel des Gesichts auf der nicht betroffenen Seite vergrößerten sich erheblich, während sie auf der betroffenen Seite deutlich abnahmen. Diese Studie ergänzt die von Dr. Alayat, M. S., et al. (2014) durchgeführten Untersuchungen, die die Wirksamkeit und Sicherheit von Hilterapia® bei der Behandlung der chronischen Bell-Lähmung belegen.
Obwohl der Artikel mit der Feststellung schließt, dass "die Hochintensitäts-Lasertherapie nachweislich eine wirksame und sichere Rehabilitationsmaßnahme ist und erfolgreich im Rahmen des Physiotherapieprogramms zur Behandlung von Patienten mit chronischer Bell-Lähmung eingesetzt werden kann", wird dieser Anwendungsbereich derzeit untersucht und gilt derzeit als Off-Label-Anwendung der Hilterapia®-Gerätelinie.

Neben der Studie der Universität Kairo gibt es eine weitere bemerkenswerte Forschungsstudie, die in der Zeitschrift "Lasers in Medical Science" veröffentlicht wurde. In dieser Studie wurde die Wirksamkeit der MLS®-Lasertherapie bei Patienten mit akuter einseitiger Gesichtslähmung unter Verwendung des robotergestützten M6-Geräts untersucht.






L'accesso alla visualizzazione dei prodotti e al materiale informativo è riservato agli operatori del settore in ottemperanza alla legislazione vigente. ASA richiede di qualificarsi come operatore del settore per procedere con la navigazione.
Decreto Legislativo 24 febbraio 1997, n°46 Articolo 21
1. E' vietata la pubblicità verso il pubblico dei dispositivi che, secondo disposizioni adottate con decreto del Ministro della Sanità, possono essere venduti soltanto su prescrizione medica o essere impiegati eventualmente con l'assistenza di un medico o di altro professionista sanitario.
2. La pubblicità presso il pubblico dei dispositivi diversi da quelli di cui al comma 1 è soggetta ad autorizzazione del Ministero della Sanità. Sulle domande di autorizzazione esprime parere la Commissione di esperti prevista dall'articolo 6, comma 3, del decreto legislativo
30 dicembre 1992, n. 541, che a tal fine è integrata da un rappresentante del Dipartimento del Ministero della Sanità competente in materia di dispositivi medici e da uno del Ministero dell'Industria, del commercio e dell'artigianato.
Some of the contents of this website cannot be disclosed in the USA and its territories and possesions, for regulatory reasons. If you are a US resident, please click on the button here below and access ASA's distributor website for North America.