MiS im Mittelpunkt: ein Informationsabend
10 November 2022 - Messen und Tagungen -
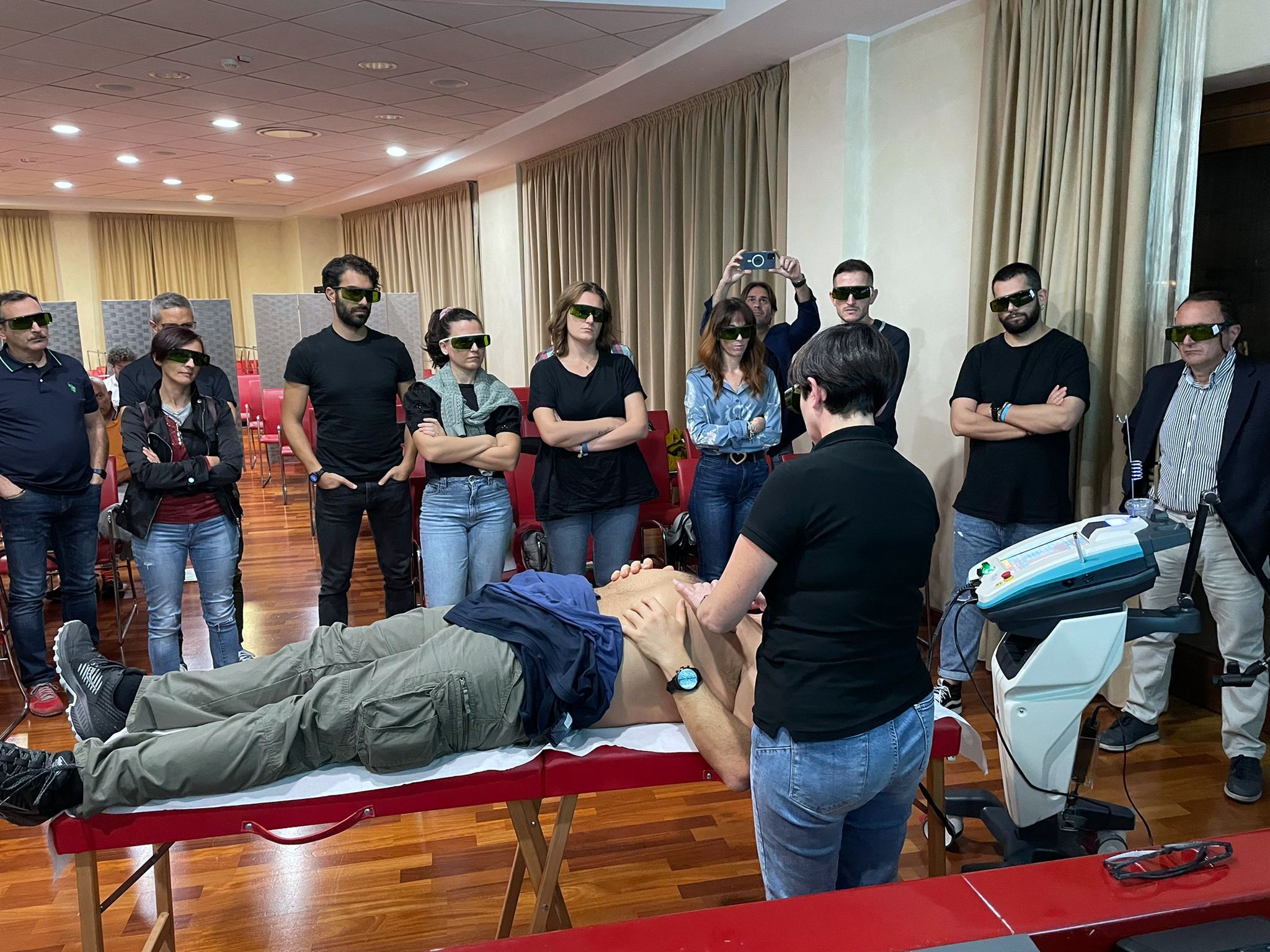
Die MLS®-Lasertherapie in der täglichen Praxis und die Verwendung von MiS bei neuropathischen Schmerzen durch die klinische Erfahrung von Mara Mezzalira (Physiotherapeutin und Inhaberin von Fisiolab 8.14) waren die Hauptthemen des ausführlichen Abends, der sich an die Besitzer des Geräts richtete und am 26. Oktober stattfand.
Unter der Leitung von Mezzalira erhielten die Teilnehmer verschiedene Hinweise zur optimalen Nutzung der MiS-Funktionen im Bereich neuropathischer Schmerzen und diskutierten Themen von vorrangigem Interesse, wie z. B. „Die Rolle des Physiotherapeuten in Italien: aktuelles Szenario und zukünftige Entwicklungen des Berufs“.
Vas Medical, langjähriger Partner aus den Abruzzen, organisierte dieses Treffen in San Giovanni Teatino, das erste einer Reihe, die für 2023 geplant ist.
“Wir sind sehr zufrieden mit den Ergebnissen dieser neuen Initiative – kommentiert Alberto Zaghetto, ASA-Bereichsleiter – der Aufbau ermöglicht es den Anwesenden, nicht nur relevante Informationen zur Verbesserung ihrer täglichen Praxis zu erhalten, sondern auch Ideen und Eindrücke auf informelle Weise auszutauschen. Die direkte Erfahrung einer Fachkraft der Branche wie Mara Mezzalira, einer langjährigen Nutzerin von MiS, ist kein zweitrangiges Element: Ihre Hinweise sind wertvolle Leitlinien für diejenigen, die sich der Therapie annähern“, schließt Zaghetto.